在临床上,胆囊癌、肝内胆管癌、肝门部胆管癌、远端胆管癌被统称为胆道癌。几种癌症类型的手术治疗因为肿瘤的解剖位置不同而有所差异,但癌症晚期的系统治疗是共通的。
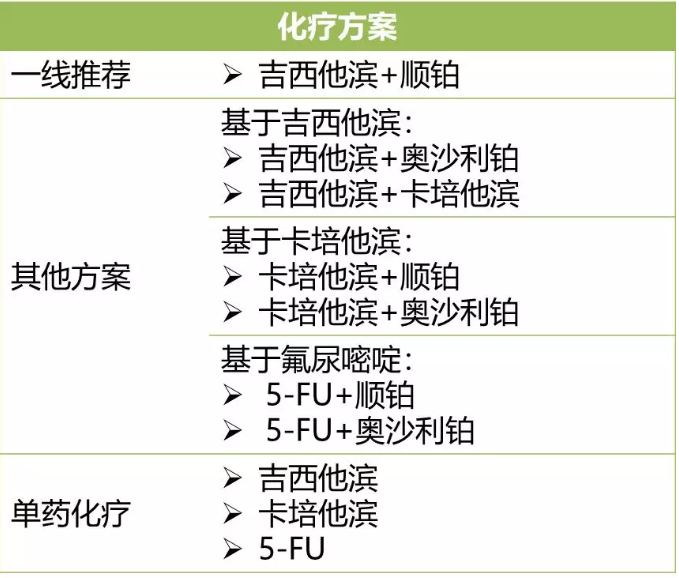
目前,国内晚期不可手术胆道癌患者的系统治疗只有化疗,一线常用化疗方案为吉西他滨联合顺铂,其他还有基于吉西他滨/卡培他滨/氟尿嘧啶的联合化疗方案。一线治疗失败后通常会换用其他方案或改用单药化疗。
编辑
请点击输入图片描述
尽管吉西他滨+顺铂的联合化疗已经是目前疗效最好的化疗,但晚期胆道癌患者的总体生存情况仍不甚理想。许多有潜力用于胆道癌的抗癌新药仍处于研发阶段。因此,越来越多的胆道癌患者开始了解、考虑并以参加临床试验的形式得到治疗。
在这里,我们为胆道癌患者梳理目前了国内正在开展的,以胆道癌为适应证的临床试验。
01 KN035
编辑
KN035
试验药物:KN035(PD-L1抗体)
治疗方案:KN035+吉西他滨+奥沙利铂
有无对照:有,对照组为吉西他滨+奥沙利铂
给药方式:KN035皮下注射,每周一次;化疗,静脉注射,21天为一周期
目标入组人数:390人
主要纳入标准
- 年龄≥18岁
- 经病理组织学或细胞学确诊的不能手术切除或转移性胆囊癌和胆管癌
- 未接受过针对不能手术切除或转移性胆道癌的系统治疗
- 肝功能Child-Pugh A级(5-6分)或者较好的B级(≤7分)
主要排除标准
- 研究者确定肝脏转移灶占肝脏总体积的50%或者以上
- 既往接受过肝移植
- 活动性脑转移或脊髓压迫
- 患有其它恶性肿瘤
- 存在HIV病史,或在首次研究药物治疗前14天内有需要系统治疗的活动性细菌或真菌感染
- 既往有间质性肺病史,药物性间质性肺病,放射性肺炎以及有症状的间质性肺病或活动性肺炎
评价
在治疗价值方面,该研究采用的是免疫检查点抑制剂(PD-L1)联合吉西他滨+奥沙利铂方案,为最前沿的免疫+化疗的组合,治疗潜力可观。试验为随机对照研究,入组患者有50%的概率进入试验组;另外50%的患者可以免费接受吉西他滨+奥沙利铂化疗,也具有现实获益。
在入组难度方面,该研究纳入标准中明确要求患者为「未接受过针对不能手术切除或转移性胆道癌的系统治疗」。
这包括几种情况:
- 未接受根治性手术的患者,且未接受过系统治疗
- 接受过根治性手术,术后未接受抗肿瘤系统治疗,出现复发或转移
- 根治性手术后接受过一种方案的辅助系统治疗,且在治疗结束后>6个月出现疾病进展;
对于胆道癌患者整个群体而言,入组该试验的窗口期较窄,入组有一定难度。但考虑到该试验治疗方案的潜在获益,参加该项临床的价值较大。
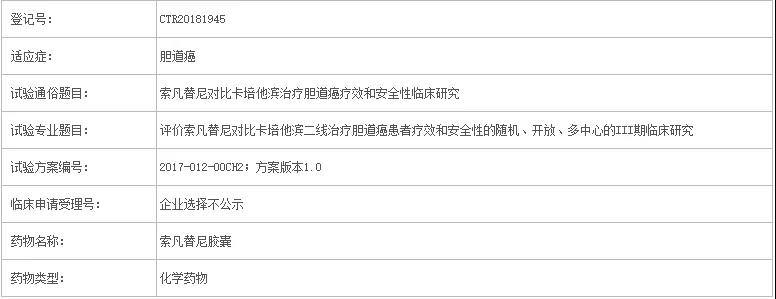
02 索凡替尼
编辑
索凡替尼
试验药物:索凡替尼(VEGFR抑制剂)
治疗方案:索凡替尼
有无对照:有,对照组为卡培他滨
给药方式:索凡替尼口服,每日一次;化疗,口服,每日两次
目标入组人数:298人
主要纳入标准
- 年龄18-75岁(含)
- 经组织学或细胞学确诊的不能手术切除或转移性胆道癌患者,包括肝内胆管癌(IHCC),肝外胆管癌(EHCC)和胆囊癌(GBC)
- 患者既往一线标准系统化疗失败。一线标准化疗方案定义为吉西他滨联合铂类的两药联合方案。
- 肝功能(Child-pugh改良分级法)评分<7分
主要排除标准
- 随机分组开始前接受过除吉西他滨联合铂类的(如氟尿嘧啶类为基础的化疗)之外的其他系统化疗(新辅助或辅助化疗,6个月内没有失败的除外);或接受过肿瘤免疫的药物治疗,如PD-1,PD-L1等;
- 研究者确定肝脏转移灶占肝脏总体积的一半或一半以上;
- 在过去5年内患有其它恶性肿瘤,根治术后的皮肤基底细胞或鳞状细胞癌,或宫颈原位癌除外;
- 已知的人类免疫缺陷病毒(HIV)感染;
- 患者目前存在中枢神经系统(CNS)转移或既往有脑转移;
评价
在治疗价值方面,该研究采用的是抗血管生成药物索凡替尼。索凡替尼(Sulfatinib)属于多靶点抑制剂,靶点为血管内皮生长因子受体(VEGFR)和成纤维细胞生长因子受体(FGFR)。与在肝癌中常用药物索拉菲尼(商品名多吉美)、瑞戈非尼(拜万戈)、仑伐替尼(乐卫玛)为同类药物。尽管为同类,但不同药物对不同种癌症的治疗效果会有差异,可以期待索凡替尼在胆道癌治疗中的疗效。
在入组难度方面,该研究明确要求患者「患者既往一线标准系统化疗失败」。该研究中,一线标准化疗方案定义为吉西他滨联合铂类的两药联合方案。包括以下两种情况:
- 吉西他滨联合铂类治疗过程中或末次治疗后6个月内出现疾病进展或毒性不可耐受
- 新辅助/辅助吉西他滨联合铂类治疗期间或治疗结束后6个月以内出现疾病进展/复发
其他备注:
- 一线的治疗用药时间需要≥1个周期
- 既往的一线标准化疗不包含抗血管生成的小分子抑制剂/单抗及肿瘤免疫相关药物
患者入组该研究的窗口期相对KN035试验较大,住院接受过吉西他滨联合铂类(顺铂/奥沙利铂)化疗,疾病进展的患者以及参加过KN035临床试验,被随机分入对照组的患者可以考虑该项临床试验。
03 Varlitinib
试验药物:Varlitinib(泛HER抑制剂),暂译威利替尼
治疗方案:Varlitinib+卡培他滨
有无对照:无
给药方式:Varlitinib口服,每日两次 ;卡培他滨口服,每日两次,持续两周
目标入组人数:30人
主要纳入标准
- 18岁(最小年龄)至 99岁(最大年龄)
- 患者患有经组织学或细胞学证实的晚期(不可切除)或转移性胆道癌,包括肝内或肝外胆管癌、胆囊癌和法特壶腹癌。
- 患者既往接受过一线(且仅有一线)针对晚期或转移性疾病的全身治疗且治疗失败,并且有疾病进展的放射学证据。此既往全身治疗必须也含有吉西他滨
- 患者无胆管阻塞的证据,除非阻塞经局部治疗得到控制,或患者的胆管树可通过内窥镜或经皮支架植入术减压,且随后胆红素降至低于1.5倍正常值上限(ULN)
主要排除标准
- 患者存在转移性脑病灶,包括无症状和得到良好控制的病灶
- 患者患有研究者认为可能危害患者安全性或研究结果可靠性的任何具有临床意义的疾病或有此等病史
- 患者有任何其他恶性肿瘤史,除非缓解期超过 1 年。(不排除经根治性治疗的皮肤癌和宫颈原位癌)
- 已知患者的 HIV 检测结果呈阳性,存在活动性丙型肝炎,存在丙型肝炎(未接受过治疗或治疗后无持续病毒学应答),或者存在乙型肝炎感染且乙型肝炎病毒脱氧核糖核酸超过 2000 IU/mL。
评价
在治疗价值方面,该研究采用国外研发的泛HER(表皮生长因子,也称EGFR)抑制剂Varlitinib联合化疗药物卡培他滨。EGFR阳性在胆道癌中较为常见,在此前EGFR抑制剂厄洛替尼联合抗血管生成药物索拉非尼治疗胆道癌的临床试验中,该组合疗法的疗效不及化疗,使得胆道癌在很长一段时间内只有化疗可用。但泛HER抑制剂Varlitinib已有较多前期临床试验数据的支持,其疗效值得期待。
在入组难度方面,该研究也招募经一线治疗失败的患者,相比于索凡替尼临床试验,Varlitinib试验对既往治疗史的要求略微宽松,仅要求经含吉西他滨的治疗方案。入组该真正的难度来自该研究计划入组的患者数量——30例,再加上该研究早在2017年末就在我国登记开展,试验名额有限。
需要说明的是,晚期胆道癌患者也有机会参加国内正在开展的其他Ⅰ期实体瘤临床试验。但相比于适应证明确的Ⅱ期、Ⅲ期临床试验,Ⅰ期实体瘤临床试验的风险更高,需要慎重考虑。
上述临床试验信息均在药物临床试验登记与信息公开平台公示。
登陆网站,输入登记号如“CTR20180332”,即可查询。