克唑替尼(Crizotinib、Crizonix、赛可瑞、Xalkori)是一种靶向ALK途径的酪氨酸激酶抑制剂。之前报道了克唑替尼在患有复发/难治性癌症儿童中I期剂量递增试验的结果,证明推荐的II期剂量(RP2D)为280 mg/m2,耐受性良好,该剂量几乎是成人标准剂量的两倍。
招募了ALK驱动间变性大细胞淋巴瘤(ALCL)和神经母细胞瘤的II期扩展队列和ALK驱动其他恶性肿瘤(包括炎性肌纤维母细胞瘤IMT)队列。本报告描述了ALCL队列和IMT患者的结果。
患者特征
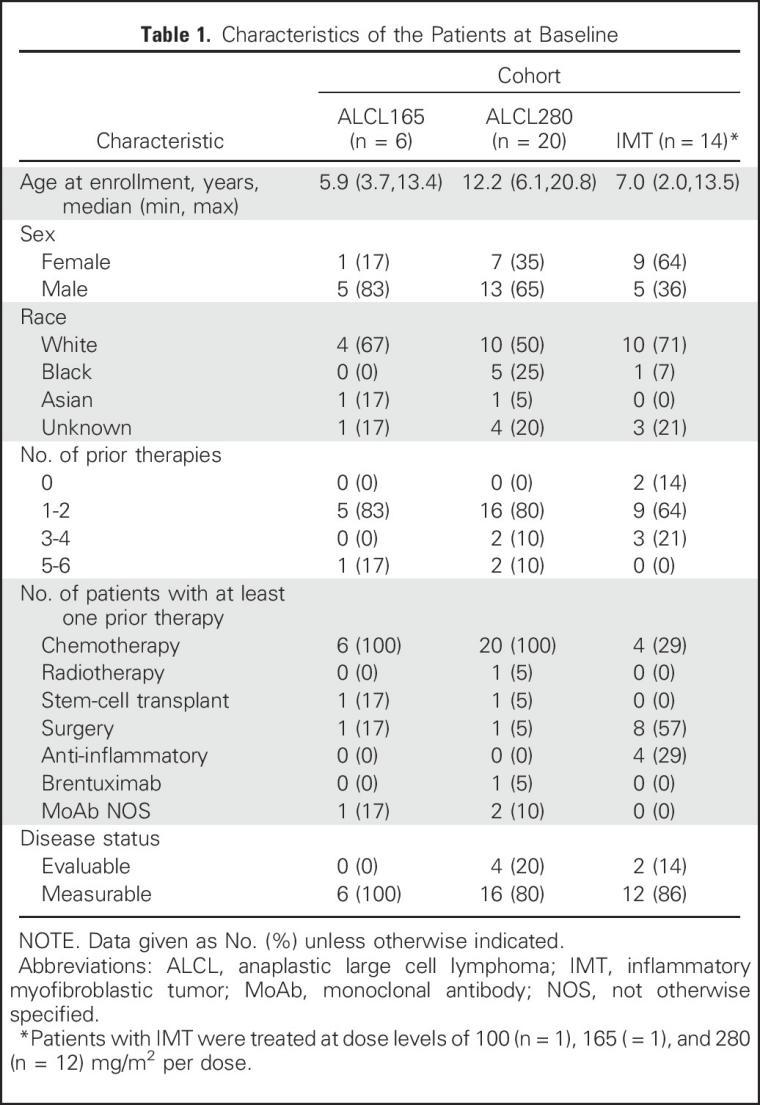
在2009年9月至2015年10月期间,26名ALCL患者和14名IMT患者参加了该研究。在26名ALCL患者中,16名(62%)参加了I期研究。其中6名以165mg/m2的剂量进行治疗,10名患者以280mg/m2的RP2D进行治疗。在I期该研究以RP2D治疗的10名患者都包括在II期研究中。其余10名ALCL患者纳入II期扩展队列并以RP2D治疗。
14名IMT患者中,有8名(57%)参加了本研究的剂量递增部分。1名以100mg/m2剂量治疗,1名以165mg/m2剂量治疗,6名以RP2D治疗。其余6名患者参加II期研究并以RP2D治疗。
ALCL患者分为两组:165 mg/m2剂量治疗(ALCL165)组和280 mg/m2剂量治疗(ALCL280)组。与ALCL165组(中位年龄,5.9岁)和IMT患者(中位年龄,7.0岁)相比,ALCL280组患者有年龄较大的倾向(中位年龄12.2岁)。所有ALCL患者至少接受过一种治疗,大部分IMT患者(86%)也接受过治疗。所有ALCL患者均至少接受过一次化疗,IMT患者只有4名(29%)接受过化疗。IMT患者接受过的最常见治疗方法是手术,14名患者中有8名(57%)接受过手术。ALCL280组有一名患者曾接受过brentuximab治疗。
临床活性
对于ALCL280组患者,客观反应率为90%;ALCL165组为83%;IMT组患者为86%。
ALCL165,ALCL280和IMT患者的中位治疗持续时间分别为2.8年,0.4年和1.6年。对于26名ALCL患者,20名患者的中央复查和中心评估反应完全一致。
以165 mg/m2剂量治疗的6名ALCL患者均有可测量病灶;5名在开始治疗后4周有初始反应的证据,2名完全反应(CR),3名部分反应(PR)。剩余1名患者病情稳定>30个周期。
以RP2D治疗的20名ALCL患者中,有18名CR或PR,其中13名患者在开始治疗后4周内出现反应。其余的在治疗第5周(n=4)和8周(n=1)内有初始反应。下图A部分显示了1名患者治疗一个周期后异常代谢活动的快速消退。
在本报告发布时,两名ALCL患者仍在接受治疗。ALCL患者停止治疗的原因如下:不良事件AE(n=2),中心判断疾病进展(n=3),医生或父母决定(n=16),未能满足研究方案的继续治疗标准(n=1),不依从(n=1),失访(n=1)。
停止研究治疗的16名患者中,12名进行干细胞移植,2名患者拒绝进一步治疗,2名患者在研究期间拒绝继续治疗,但继续使用商品克唑替尼。由于AE(中性粒细胞减少症)而停止研究治疗的一名患者,在克唑替尼第一个治疗周期后也进行了干细胞移植。
在12名CR或PR的IMT患者中,7名开始治疗后4周内、2名在8周内、3名在20周内有初始反应。在14名IMT患者中,3名进行PET影像学检查:2名患者在4周时按照RECIST标准评估获得PR,在同一时间点通过功能代谢成像评估获得CR,但未实现解剖学CR;一名患者在12周时PR,在第40周时CR,但在12周时通过18F-FDG PET影像学检查评估获得CR。一名患者仅进行了18F-FDG PET/CT影像学检查,并且根据PET评估其反应。
在本报告发布时,两名患者仍在进行研究治疗。IMT患者停止治疗的原因如下:包括重复性4级绝对中性粒细胞计数和下肢水肿在内的AE(n=4),医生或父母决定(n=5),完成24个治疗周期(n=1),不依从(n=2)。
本内容为医伴旅版权所有,转载请注明出处。
医伴旅:寻找优质医疗资源,伴您走上康复之旅





