20190813 周二
膳食脂质在食物过敏中的作用
Crit Rev Food Sci Nutr (IF: 6.704,1区)
推荐|史晨杉
研究背景
工业化国家的食物过敏患病率正在上升,但这种发病率上升的机制尚不完全清楚。环境因素被认为在过敏性疾病中起作用,包括生活方式影响,例如饮食。过敏原和脂质之间存在密切关系,许多过敏原蛋白具有结合脂质的能力。膳食脂质对先天免疫的细胞发挥促炎或抗炎功能,并影响抗原呈递给适应性免疫的细胞。除了改变蛋白质的免疫刺激性质外,脂质还改变其消化率和肠道吸收,改变过敏原的生物利用度。本研究概述了膳食脂质在食物过敏中的作用,同时考虑到流行病学信息,体内,离体和体外模型。还讨论了高脂饮食,肥胖和过敏之间的联系。
研究内容
1 多不饱和脂肪酸,炎症和过敏预防
n-6 PUFAs的下游代谢物通常被描述为促炎物质,而n-3 PUFAs的下游代谢物有可能解决炎症并改善过敏症状。相当多的观察性研究显示,怀孕期间母体鱼摄入量,母乳中EPA百分比和儿童过敏性疾病风险降低之间存在有益的关联。关于孕期和哺乳期,婴儿期或儿童期鱼油补充效果的研究强调了n-3多不饱和脂肪酸在儿童特应性中的治疗或预防临床效果的相互矛盾的结果。无论如何,目前关于产前补充鱼油对过敏性呼吸道疾病的长期预防潜力的研究并没有提供决定性的结果。有趣的是,n-3 PUFAs的潜在健康益处并不仅仅与鱼或鱼油的消耗有关。在农场长大的孩子比在非农业环境中长大的孩子患过敏的风险要低得多。
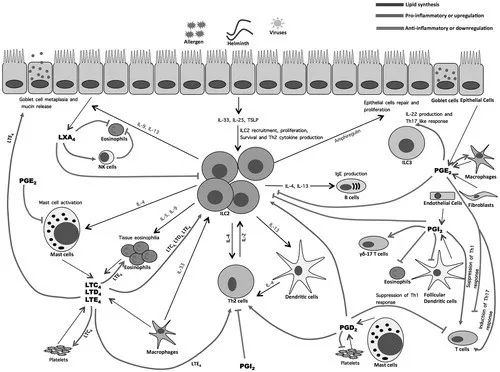
2 多不饱和脂肪酸对先天性和适应性免疫系统细胞的影响
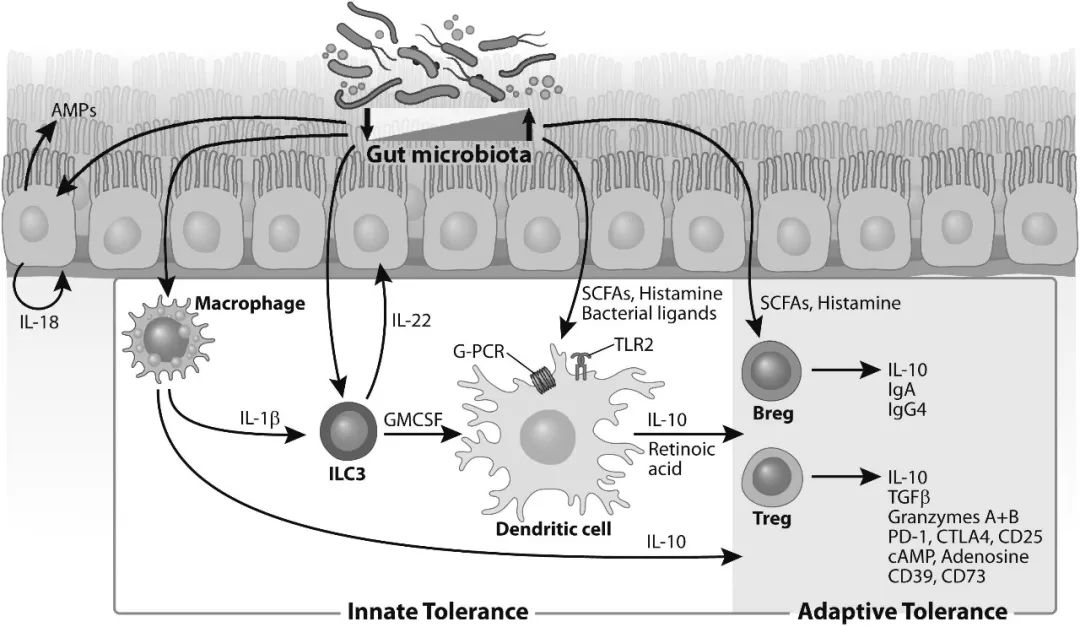
已经证明n- 3 PUFA对先天免疫系统的细胞(巨噬细胞和树突细胞,DC)发挥免疫调节作用。n- 3多不饱和脂肪酸的这些作用至少部分是由核因子κB(NF-κB)途径的失活介导的,该途径控制参与细胞因子,趋化因子和粘附的参与的促炎基因的表达。PUFAs也是过氧化物酶体增殖激活受体γ的活化剂。n- 3 PUFA对离体 T细胞增殖的饮食效应取决于刺激倾向于使T细胞偏向假定的Th1样或Th2样子集,特别是降低用Th1- 处理的CD4 + T细胞的活力。
3 磷脂和过敏原的蛋白水解降解的敏感性
脂质结合蛋白与膳食或内源性分泌的PLs(磷脂)的相互作用对其胃肠稳定性和随后的免疫反应性产生重要影响。PC(磷脂酰胆碱)以及其他PL已经显示出在体外胃消化中保护某些食物过敏原,例如α-乳白蛋白。
4 甘油脂和肠道吸收
小肠的吸收性肠上皮细胞将甘油脂(GL),主要是甘油三酯(TG),PL,胆固醇和蛋白质组合成称为乳糜微粒的脂蛋白颗粒,其通过淋巴管和全身循环将吸收的脂质转运到不同的组织。与膳食长链TG(> 12C原子; LCTs)不同,大量过敏性食物如花生或牛奶,短链和中链TG(MCTs)不需要乳糜微粒吸收,因此不会诱导乳糜微粒形成。
5 通过食物的脂质部分激活免疫应答
许多吸入剂和食物过敏原都有与脂质结合的能力。脂质除了改变完整蛋白质结构的保存程度外,还可能改变蛋白质的免疫调节特性。另一种参与T细胞识别脂质结合蛋白的先天途径与CD1有关,CD1是一种由APCs和上皮细胞表达的非多态性MHC类i分子,具有脂质抗原,使其具有免疫原性。
6 高脂肪饮食,肠内稳态和食物过敏
一些研究强调了高脂肪饮食和细菌之间的相互作用,以促进肠道中促炎症的变化。
7 肥胖与过敏之间的关联
从长远来看,高脂肪饮食导致脂肪储存和肥胖。在过去的三十年中,过敏性疾病和肥胖症患病率的平行上升表明它们之间存在因果关系。事实上,越来越多的流行病学证据将肥胖与哮喘联系起来,尽管与其他特应性疾病(如过敏性鼻炎,皮炎和食物过敏)的关联不太明显。
研究结论
过敏性食物通常具有高脂质含量,并且许多过敏性蛋白质具有结合脂质的能力。除了改变蛋白质的免疫刺激性质外,膳食脂质还改变其消化率和肠道吸收,改变过敏原的生物利用度。另一方面,膳食暴露于高脂肪饮食会影响微生物群的组成,直接影响过敏的发展。此外,肠道微生物群落的变化改变了营养素的能量吸收,而肥胖,赋予炎症介质和免疫细胞额外的影响。未来的临床和基础研究需要揭示脂质导致过敏的复杂机制。增加对膳食脂质,肥胖和过敏倾向的质量和数量的关联的理解将允许未来预防和治疗食物过敏的方向。