一、病例简介
患者,女,56岁,己婚,1-0-1-1,因“发现子宫肌瘤20余年”入院。
现病史:20年前患者当地医院体检,查妇科超声提示“子宫肌瘤,大小约1-2cm”(未见报告单),当时无月经改变及腹痛腹胀等不适,具体诊治不详,建议定期复查。患者遂每年复查,盆腔包块逐年增大,2014年患者绝经,绝经后至今包块仍缓慢增大,无异常阴道流血,无尿频尿急,无腹痛便秘等不适主诉。2018-12及2019-4患者均在我院复诊,超声提示“子宫多发肌瘤,较大位于子宫前壁,肌瘤大小由6.1cm*5.9cm*6.2cm增大至7.5cm*6.7cm*7.4cm”。无阴道流血,无腹胀腹痛,无尿频尿急等不适,诊断“盆腔包块(子宫肌瘤?)”,建议住院手术。患者病程中无畏寒发热,无胸闷气促,无咳嗽咳痰,无恶心呕吐,无腹痛腹胀,无阴道流血流液,无尿频尿急,无肛门坠胀等不适。今为进一步手术,收住入院。
既往史:外院确诊糖尿病4年,目前予“二甲双胍0.5g口服1/日+比格列酮片1片口服1/日+格列美脲片1片口服1/日”控制血糖,自诉监测空腹血糖在6.8mmol/L-8mmol/L,餐后血糖在8mmol/L-9mmol/L。余无特殊病史及手术外伤史。
月经史:初潮15岁,5-6/30天,51岁绝经。平素月经规则,绝经后无异常阴道流血流液。
婚育史:21岁结婚,丈夫体健,1-0-1-1,工具避孕。
体格检查:生命体征平稳,心肺听诊无殊,腹软,无压痛及反跳痛,双下肢无水肿。
妇科检查:双合诊,外阴:已婚已产式,阴道:通畅,无异常分泌物,宫颈:萎缩,光,无触血,无赘生物,子宫:前位,如孕3月,活动可,无压痛,附件:双附件未及包块及压痛,其他:无殊。
辅助检查:入院查大小便常规、乙肝三系、STD、甲状腺功能、肿瘤指标,心电图,胸片,宫颈TCT,HPV检查未见明显异常。入院血常规:白细胞计数6.0*10^9/L,中性粒细胞分类66.1%,血红蛋白98.0g/l,血小板计数419.0*10^9/L;血沉96MM/H;凝血功能常规检查:纤维蛋白原6.38g/l;生化全套:白蛋白36.7g/L,超敏C-反应蛋白85.9mg/L;血降钙素原0.05ng/mL。盆腔MRI增强扫描示:子宫前倾位,明显增大变形,子宫前壁见大小约9.2*7.4*7.5cm占位,见包膜,T1WI呈等信号,内见片状及条索状稍高信号影,T2WI呈稍低-等信号,DWI信号混杂,部分呈高信号,增强扫描不均匀强化,宫腔受压变形。双侧卵巢显示不清。盆腔淋巴结未见明显肿大。诊断结果:子宫肌瘤伴变性考虑。
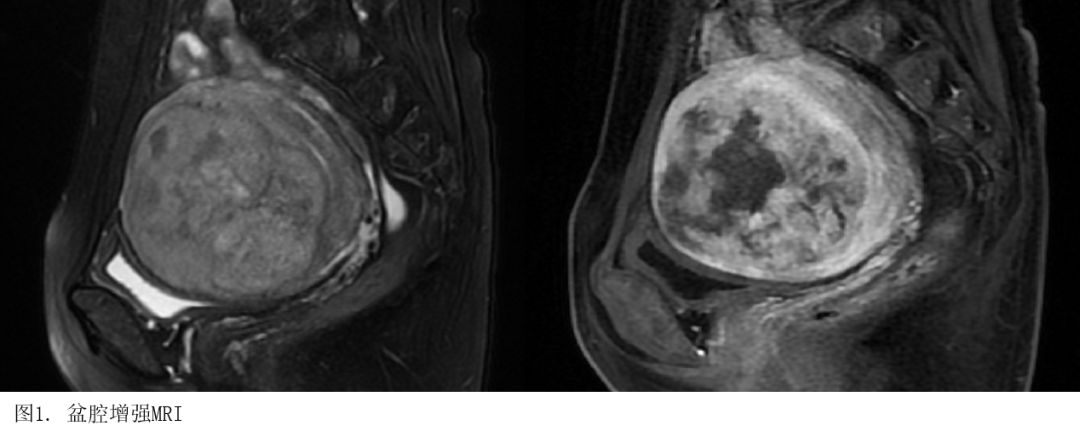
初步诊断:子宫肌瘤,轻度贫血,2型糖尿病
诊疗计划:1、患者CRP、ESR升高,完善病原学培养;2、预防性抗生素使用48小时,择期复查感染指标;3、限期行经腹全子宫切除术。
-----
-----
二、诊治经过
术前情况:入院后患者体温正常,完善相关检查,提示血常规(WBC、N%),PCT均在正常范围,但CRP、ESR较高,原因不明,进一步完善血、尿、宫颈分泌物培养,结果回报均阴性,肺部及全腹CT扫描未见明显异常。 予静脉抗生素使用预防感染48小时后,复查血常规:白细胞计数5.9*10^9/L,中性粒细胞分类66.8%,血红蛋白96.0g/l,血小板计数410.0*10^9/L;超敏C-反应蛋白74.7mg/L;血沉101MM/H。呈上升趋势,考虑肌瘤变性或恶变导致CRP及血沉升高,亦不排除其他感染性疾病可能,故予相关科室会诊,排除绝对手术禁忌后,限期行 经腹全子宫切除术+双附件切除术。
手术经过:患者在硬膜外麻醉下行“经腹全子宫切除术+双附件切除术”,术中见: 盆腔内见淡血性液体10ml,予生理盐水冲洗盆腔,留取腹水冲洗液送细胞学检查,子宫前位,增大如孕3月大小,表面光滑,质地偏硬,双侧卵巢萎缩,大小约2*2*1cm,外观无殊,双侧输卵管走行自然,质地柔软,伞端粘膜可见;部分肠管与子宫左侧后壁膜状粘连,子宫直肠陷凹存在,探查双侧宫旁组织无增厚,探查阑尾、大网膜、胃、肝、脾、肠管等处均无异常病灶,盆腔和腹主动脉旁淋巴结未及明显肿大。遂行上述手术。操作:大纱垫排肠,两把长弯血管钳钳夹两侧宫旁组织,上提子宫,充分暴露子宫。钳夹左侧子宫圆韧带中内 1/3 处并切断,盆腔侧残端丝线缝扎牵引,于左侧阔韧带无血管区打孔,予以钳夹左侧卵巢漏斗韧带,离断,盆腔侧断端7号丝线缝扎及套扎各一道。同法处理对侧。顺势打开左侧阔韧带前叶,打开子宫膀胱反折腹膜,钝锐性分离膀胱与宫颈间致密组织,下推膀胱至宫颈外口水平以下1cm。打开左侧阔韧带后叶,暴露子宫血管,在子宫峡部水平钳夹左侧子宫动静脉,切断,1-0可吸收线缝扎两道,同法处理右侧子宫血管。紧贴宫颈分次钳夹、离断左侧宫颈主骶韧带,残端分别缝扎。同法处理右侧相应组织。盐水巾保护,沿阴道穹隆环切,完整切除全子宫及双附件。阴道内塞 PVP 纱布1条(术毕取出),阴道残端常规PVP棉球消毒三遍,用1-0可吸收线连续缝合阴道断端,并加固缝合数针。台下助手剖解标本:子宫增大,如孕3+月大,Y形剖检见子宫内膜菲薄,子宫前壁见9cm*8cm*8cm的肌瘤样包块,质硬,突向宫腔,质地不均,部分质韧,部分成胶冻状,剖面颜色不均,可见淡黄色区域以及白色区域,部分白色区域可见纤维束样结构,肿块剖面旋涡状结构不明显。双侧卵巢偏小,外观无殊;双侧输卵管外观无殊。标本送快速冰冻。术中病理结果回报:子宫平滑肌肿瘤伴坏死及异型,平滑肌肉瘤待排。术中予患者家属沟通,目前已行全子宫及双附件切除,盆腔肿块局限子宫体,盆腔内未见明显异常病灶及肿大淋巴结,即使术后常规病理提示子宫肉瘤,目前手术范围已足够。家属知情理解签字拒绝行盆腔淋巴结切除,要求原方案完成既定术式。遂常规关腹,检查各残端和创面无活动性出血,1-0 可吸收线缝合盆底腹膜。5%PVP-I及生理盐水冲洗盆腔,检查盆腔内无活动性出血,双侧输尿管蠕动正常。清点纱布和器械无误后,常规逐层关腹, 皮肤切口4-0可吸收线皮内缝合。手术经过顺利,术中出血100ml。
术后情况:术后患者恢复可,术后第一天复查血常规: 白细胞计数7.1*10^9/L,中性粒细胞分类79.4%,血红蛋白103.0g/l,血小板计数387.0*10^9/L;超敏C-反应蛋白107.0mg/L;血沉91MM/H。术后第三天复查:超敏C-反应蛋白14.5mg/L;血沉67MM/H。术后第7天出院,嘱出院后3月门诊随访。 术中腹水细胞学检查:未找见癌细胞。术后常规病理提示:子宫间叶源性恶性肿瘤,结合免疫组化,符合恶性炎性肌纤维母细胞瘤;子宫内膜老年性,子宫颈粘膜慢性炎,阴道前后壁粘膜慢性炎,双侧输卵管及卵巢组织双侧宫旁及卵巢血管均阴性。备注:建议ALK基因重排检测。
-----
-----
三、病例分析
知识点1
一、子宫肉瘤的定义及临床表现
子宫肉瘤占女性生殖器恶性肿瘤的1%,占子宫恶性肿瘤的3%~7%,子宫肌瘤恶变占所有子宫肌瘤的0.5%,子宫肉瘤的分类包括子宫平滑肌肉瘤(uLMS)、子宫内膜间质肉瘤(ESS)、未分化子宫肉瘤(UUS)和其他罕见类型如腺肉瘤,横纹肌肉瘤等。ESS可进一步分为 低级别ESS(LGESS)、高级别ESS(HGESS)。从组织来源上看,uLMS可能来源于子宫肌层最为常见;ESS和UUS可能来源于子宫内膜。其临床表现主要为括异常阴道出血、可触及的盆腔肿块以及盆腔疼痛。子宫肉瘤的术前诊断较为困难,对短期内明显增大的子宫肌瘤应引起重视,尤其在绝经后妇女。
二、子宫肉瘤的诊断
有研究认为术前结合患者年龄、LDH明显升高、MRI多序列扫描如弥散加权项以及增强扫描对肿瘤的部位及性质判断可能有帮助,对于异常阴道流血患者可采取分段诊刮以及子宫内膜细胞学检查结果进行判断,但由于子宫肌瘤存在多种变性,对于子宫肉瘤目前仍然没有较为敏感的无创性检查。
三、子宫肉瘤的治疗
子宫肉瘤的治疗以手术为主,内分泌治疗,化疗或(和)放疗为辅。子宫肉瘤的标准术式是全子宫及双附件切除术,是否行盆腔或腹主动脉旁淋巴结清扫尚存有争议。(1)局限于子宫者:全子宫+双附件切除;不能手术者:盆腔放疗±阴道近距离放疗和(或)全身系统性治疗。(2)子宫外有病灶者:全子宫+双附件切除+转移病灶切除,包括转移淋巴结切除;不能手术者:盆腔外照射放疗±阴道近距离放疗和(或)全身系统性治疗。某些特殊情况下,如宫颈肌瘤肉瘤变或肉瘤侵及子宫颈,可行广泛性全子宫切除术,必要时行盆腔及腹主动脉旁淋巴结切除术。由于LGESS患者保留卵巢复发率极高,故建议双侧附件切除,也不提倡术后雌激素替代治疗。对于年轻的、ER阴性的早期uLMS患者,可谨慎保留一侧附件。子宫肉瘤的手术强调完整切除子宫肿瘤,切忌在腹腔内施行肿瘤粉碎术。
-----
-----
分析1
该患者绝经5年,无任何临床症状,术前LDH、肿瘤标记物均正常,影像学未提示肉瘤征象,但结合患者绝经后子宫肌瘤仍有增长,且近两年增长明显,子宫肉瘤不能排除,故需避免子宫粉碎,即使选择全子宫切除术,患者子宫体积较大,经阴道取出困难时仍需切割子宫,分块取出,仍有肿瘤播撒可能。近年来采用的封闭式微创粉碎技术或可解决该问题,但仍缺乏长期安全的随访数据,且封闭式专用取物袋价格昂贵,较多医院或医生发明并开展“自制取物袋内粉碎技术”,但其意义多在于粉碎术后盆腔更“清洁”或便于清理,粉碎过程中存在取物袋破裂风险,故是否在高度怀疑子宫肉瘤的患者中推广,仍待商榷。故针对本例患者,我们仍建议手术方式选择为经腹全子宫切除术+双附件切除。
-----
-----
知识点2
一、什么是炎性肌成纤维细胞瘤?
炎性肌成纤维细胞瘤(IMT)是一种间充质肿瘤,最常见于肺部或腹部、骨盆和腹膜后的软组织。最初被认为是良性肿瘤,但随着复发和转移病例的出现,目前被分类为中等恶性潜能的肿瘤。根据WHO骨与软组织肿瘤分类IMT复发率约为25%,转移率约2%。大约50%的炎性肌纤维母细胞瘤有涉及间变性淋巴瘤激酶基因(ALK)的重排,该基因位于染色体2p23,近期研究在ALK基因重排阴性的病例中发现ROS1,PDGFRB,RET和NTRK1等基因的重排。
二、女性IMT的特点
女性生殖道中IMT最常见的发生部位为子宫体,其次为宫颈,子宫部位的肌纤维母细胞瘤不常见,目前仅见数十例个案报道。年龄从6岁到73岁不等,最常见的临床症状为盆腔包块相关症状,如腹部不适、腹胀、骨盆疼痛、压力性尿失禁等,月经异常也是常见主诉,部分患者会出现疲劳、发热、厌食和体重减轻的消耗性症状。 辅助检查可出现炎症相关表现,如轻度白细胞升高,白介素6水平升高,血沉加快,C反应蛋白升高、血小板增多等。 血清肿瘤标志物可在正常范围内。部分研究显示子宫部位IMT可能与妊娠存在一定关联,除子宫体,妊娠期IMT也可发生与胎盘部位。子宫部位的IMT大体标本外观表现为大小不等的粘膜下肿块,有时有蒂,也可类似肌壁间肌瘤累及肌层的浆膜下包块。剖面成不均匀的黄褐色或白色,中间有黄色区域,质地不均匀,部分质韧,部分质软,部分呈胶冻状,可见囊性改变、出血灶和坏死区。一些IMT可能有典型的平滑肌瘤外观,表面呈棕褐色白色,偶尔有粘液样改变。
三、IMT诊断及治疗
超过70%子宫部位的IMT表现为ALK蛋白异常染色或ALK基因重排阳性。因此可以通过ALK蛋白的免疫组化染色或ALK重排基因荧光原位杂交及ALK基因测序来诊断IMT。IMT为惰性肿瘤,有相对较高的复发率和较低的转移率,一项研究分析了13例子宫部位的IMT,中位随访时间31个月,13名患者中8名无病生存,1名患病生存,3名因病死亡,1名失访。该研究发现瘤体直径大于10.5cm,重度核不典型,核分裂大于18/10个高倍镜视野以及淋巴管侵犯可以预测肿瘤恶性行为,瘤体直径大于8cm是肿瘤复发的高危因素。ALK阴性肿瘤更具有转移倾向,但ALK表达并不能预测复发。手术治疗仍是子宫部位IMT的首先治疗,手术以完整去除肿瘤为目的,无生育要求患者可考虑行全子宫及双附件切除术,目前尚无术后辅助治疗的循证医学依据,对于恶性程度高、复发及无法切除的肿瘤且ALK基因重排阳性病例可考虑使用酪氨酸激酶抑制(crizotinib)剂靶向ALK治疗。
-----
-----
分析2
本例患者以发现盆腔包块为主诉,术前发现CRP,血沉,血小板,纤维蛋白原等炎症相关指标明显升高,但未发现明确感染病灶,应用抗生素治疗后上述指标并无明显改善,但手术后第三天复查CRP及血沉较前明显下降,故该患者临床表现符合IMT,手术已完整切除肿瘤,且该患者未发现子宫以外的病灶,故认为目前患者目前暂不需要其他辅助治疗,但由于该患者存在肿瘤直径较大的高危因素,在手术完整切除肿瘤后仍应密切随访,上述炎症相关实验室指标可作为随访及预测肿瘤复发指标。
-----
-----
总结
子宫肉瘤虽然发生率较低,但在妇科微创手术广泛应用的背景下仍需引起重视,其临床表现与子宫平滑肌瘤常常难以鉴别,随着妇科手术医生内镜技术不断提高,并热衷于新的“挑战”,在某种程度上抱有“侥幸”心理。因“子宫肌瘤粉碎”而导致的恶性肿瘤播撒相关事件在美国多有报道,并引起一系列的政策警告,甚至矫枉过正。针对本病例,仔细询问病史,完善辅助检查,对于肌瘤变性且绝经后瘤体持续增大的患者,选择合适的手术方式及途径,仍是一线临床医师需认真面对的抉择。


