骨质疏松症 (OP) 是以骨量减少、骨组织微细结构退化、破坏, 导致骨脆性和骨折危险性增加为特征的一种全身性、代谢性骨骼疾病。年龄逐步增长或女性进入绝经期, 体内性激素水平的骤减、钙调节激素的分泌紊乱及微量元素的摄入不足是导致老年和绝经女性原发性OP的重要病因。随着经济的发展和医疗技术的进步, OP治疗花费亦在逐年增加。
根据2009年国际骨质疏松症基金会首次在亚洲14个国家开展的骨骼健康状况和OP的综合性研究报告指出:至2020年, 中国OP或低骨密度患者将达到2.866亿人次, 而因骨质疏松引起的髋部骨折治疗经费将达到850亿元,至2050年患者人数则将跃升至5.333亿;治疗经费更剧增至1.8万亿元。
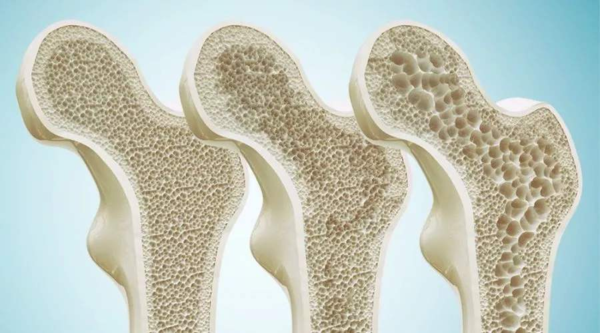
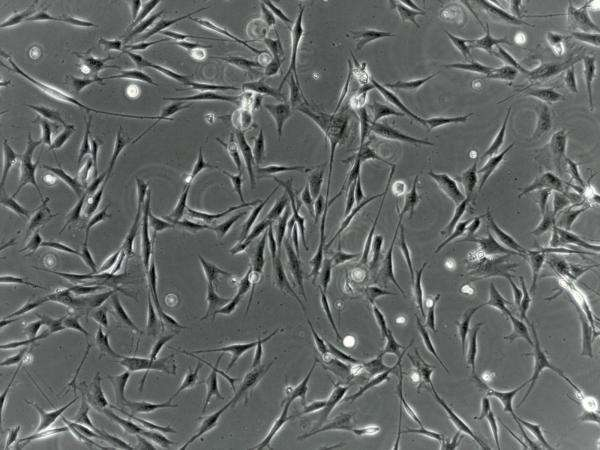
因此世界卫生组织 (WHO) 将OP列为心血管疾病之后的第二位健康问题, 但目前尚未完全阐明OP的发生机制。间充质干细胞 (MSCs) 是来源中胚层存在于骨髓及多种组织中的多向分化的一类干细胞, 可向成骨细胞、脂肪细胞、软骨细胞及神经细胞等分化。MSCs符合干细胞所特有的自我更新和多向分化的潜能, 又不具有致畸胎瘤的风险;MSCs可分泌多种生长因子和细胞因子, 利于受损组织进行修复, 如MSCs通过分泌骨形成蛋白 (BMPs) 进行软骨、骨及肌腱等修复。
目前公认的骨质疏松症发病机制是成骨细胞和破骨细胞在骨重塑过程中失衡,成骨细胞数量和活性降低,破骨细胞数量增加、功能活跃,导致骨形成减少,骨吸收增加,使骨吸收速率超过骨形成速率,造成骨质疏松。成骨细胞起源于骨髓腔的一种多能干细胞———骨髓间充质干细胞(MSC)。
间充质干细胞的功能直接影响成骨细胞的数量和活性。有学者对10例17岁至90岁志愿者的间充质干细胞分化培养成骨2周,,发现年龄较大者(≥55岁)的间充质干细胞成骨分化能力显著下降。骨髓间充质干细胞的成骨分化能力与鼠的年龄和干细胞传代次数呈线性相关,干细胞成骨分化能力随年龄和传代次数增加而下降。
原发性骨质疏松症的发病机制大多与骨髓间充质干细胞的功能异常、细胞衰老相关。由于MSCs具有广泛的获得性并拥有多向分化的潜能, 且多项研究表明MSCs能够在机体组织损伤、生长及愈合中进行替换和更新体内细胞。因此, 被认为具有较强促再生能力的MSCs在治疗OP中具有广泛的应用前景。
作为脂肪细胞和成骨细胞的同源体, MSCs数量的减少或功能的缺损, 会直接引起OP, 因此, 系统或局部移植正常功能的MSCs被认为对治疗OP具有一定的疗效。MSCs移植后可直接增加骨内MSCs总数量, 提高成骨分化, 更为重要的是可分泌多种趋化因子, 这些趋化因子对于OP引发的骨折具有重要的治疗意义, 该治疗方法因其具有传统治疗方法不可比拟的优势,如治疗时间短、方式便捷等。