毋庸置疑,免疫治疗已成为癌症精准医疗中的一大热点,并已逐步发展成为继手术、化疗和放疗后的第四种肿瘤治疗模式。至此跨年之际,Nature Reviews Clinical Oncology杂志以肿瘤免疫疗法为主题,精选了近年来肿瘤免疫研究中的经典图片。测序中国对其进行了编译整理,内容如下:
图1
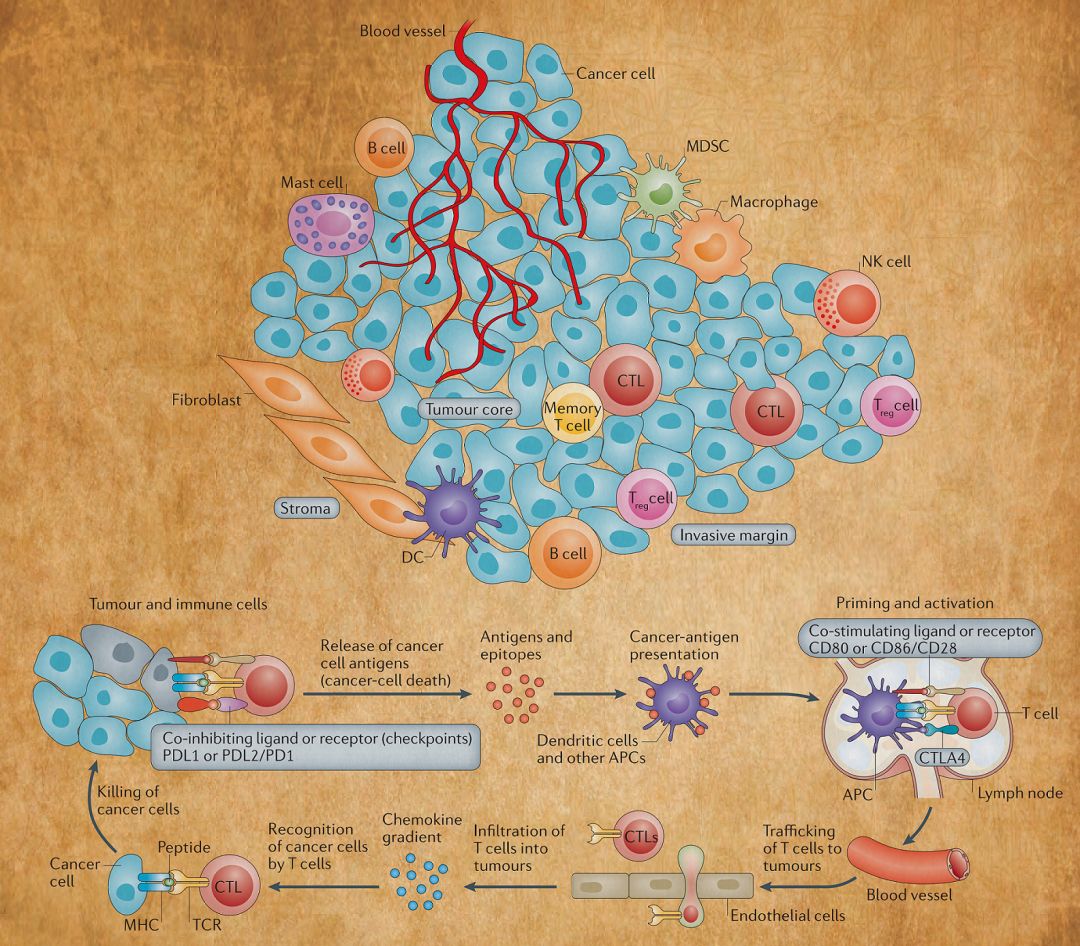
肿瘤免疫系统是肿瘤免疫应答、免疫逃逸和肿瘤发生发展等相互关系的研究基础,对肿瘤的免疫诊断和防治有极其重要的作用。图1显示了肿瘤免疫系统中,来自适应性和先天免疫系统的多种免疫细胞类型。癌细胞可导致机体的免疫反应,癌症免疫周期主要包括:抗原生成,树突状细胞向T细胞呈递抗原,启动并激活针对癌症特异性抗原的效应T细胞,T细胞转运到肿瘤部位,癌细胞被识别并被杀死。
图片来源:
Hackl, H., Charoentong, P., Finotello, F.& Trajanoski, Z. Computational genomics tools for dissecting tumour–immune cell interactions. Nat. Rev.Genet. 17, 441–458 (2016)
γδT细胞的抗肿瘤生物学研究
图2
在免疫系统中,T淋巴细胞(简称T细胞)发挥着重要的免疫功能。T细胞表面存在诸多标记,如T细胞受体(TCR)、白细胞分化抗原(CD)等,根据T细胞表面TCR的类型,可将T细胞分为αβT细胞和γδT细胞两类。其中αβT细胞占T细胞总数的95%以上;γδT细胞数量较少,具有抗感染和抗肿瘤的作用。图2反应了γδT细胞的抗肿瘤功能及其调控。γδT细胞通过TCR和自然杀伤细胞受体(NKR)直接识别肿瘤细胞,通过各种机制介导肿瘤细胞死亡,包括产生抗体依赖性细胞毒性和干扰素-γ(IFNγ)。γδT细胞的抗肿瘤特性主要由白介素15(IL-15)、IL-2、IL-18和IL-21增强,其杀伤能力则受到肿瘤微环境中表观遗传药物或分子因素的抑制。
儿童癌症免疫疗法
图3
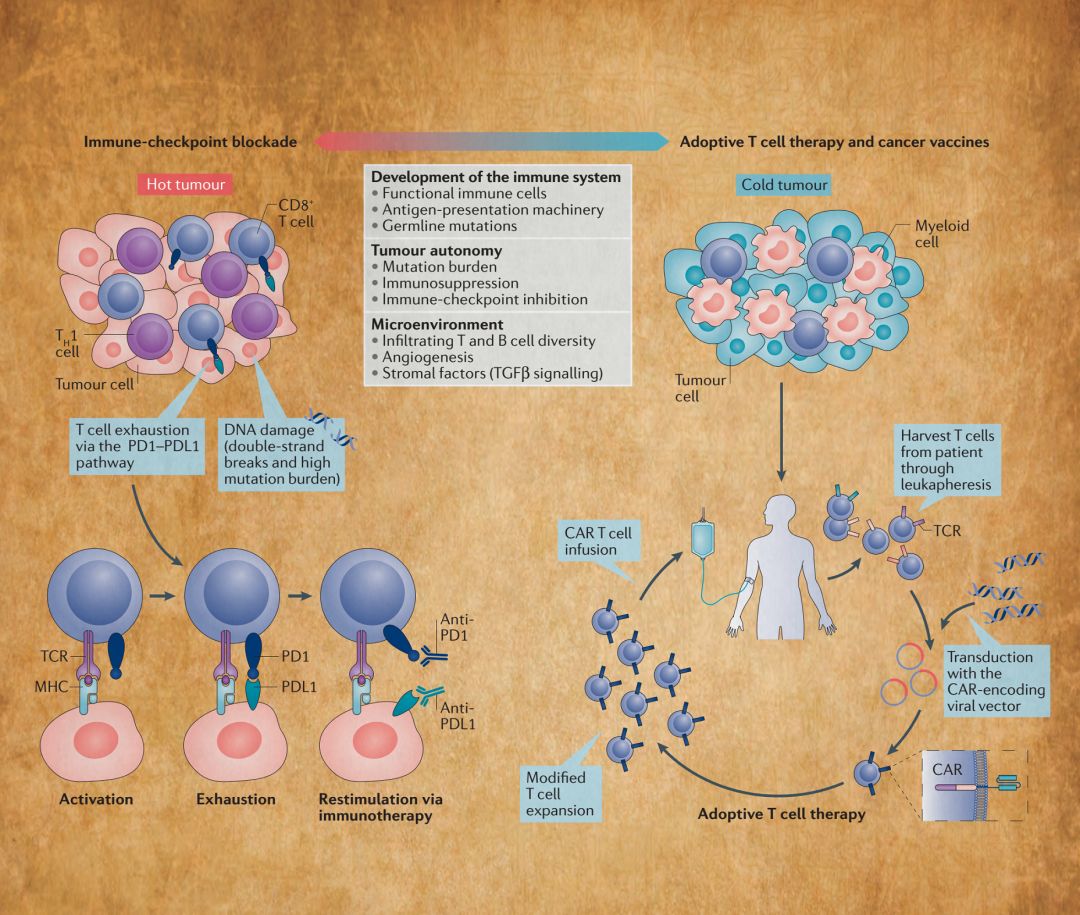
图3总结了目前正在试验的儿童癌症的各种免疫治疗方法。大多数儿童肿瘤被认为是“冷肿瘤”(右上)。基于细胞疗法,包括嵌合抗原受体(CAR)T细胞疗法(右下),正在探索作为儿童癌症免疫治疗的潜在选择。左图代表以炎性T细胞微环境为特征的“热”肿瘤,并阐明了免疫检查点抑制剂增强肿瘤部位的T细胞抗肿瘤活性的机制。
肿瘤微环境代谢
图4
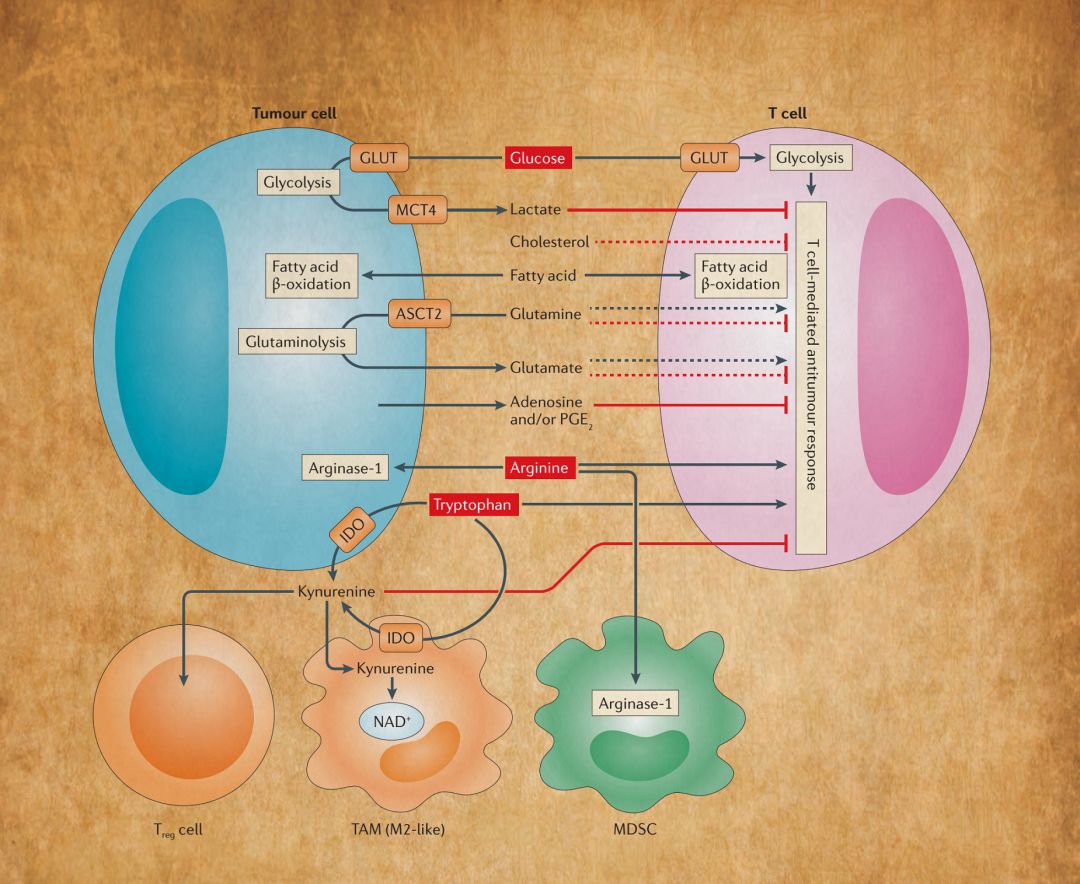
图4描述了在肿瘤微环境中活跃的代谢途径及其对抗肿瘤免疫力的影响。肿瘤细胞会产生大量的能量,并产生葡萄糖缺乏和富含乳酸的肿瘤微环境(TME),进而损害T细胞功能和抗肿瘤免疫反应。同时,T细胞和肿瘤细胞之间的氨基酸竞争也可以抑制抗肿瘤免疫力。在TME中,T细胞脂肪酸的可用性也受到肿瘤细胞竞争的影响。肿瘤细胞和其他免疫调节细胞产生的其他代谢物,也与T细胞介导的抗肿瘤反应抑制有关,包括腺苷和前列腺素E2(PGE2)。
肿瘤免疫分类
图5
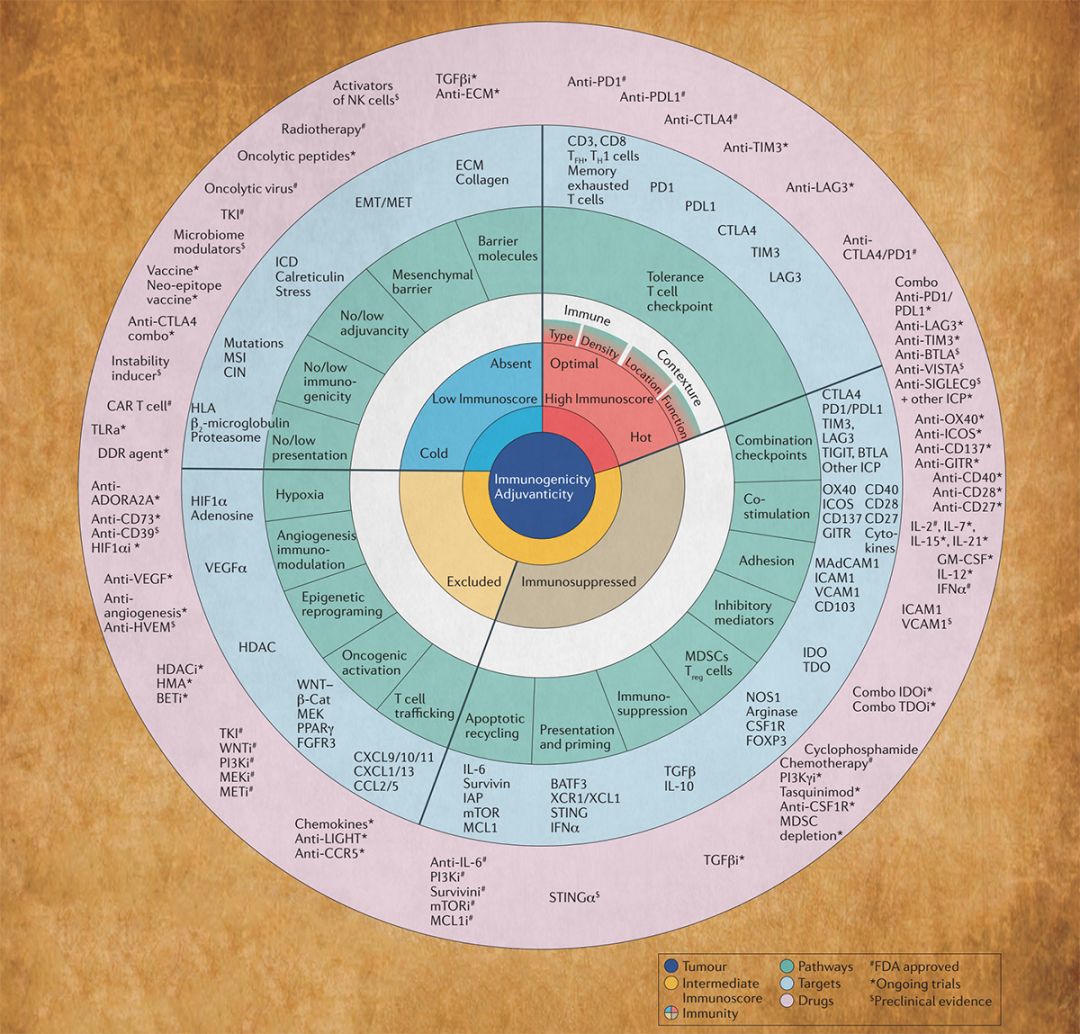
根据T细胞的存在和分布,肿瘤可以分为四种主要的亚型:热肿瘤、冷肿瘤、免疫阻隔型肿瘤、免疫抑制型肿瘤。图5概述了已鉴定不同类型肿瘤的免疫图谱的主要成分、途径和特征(绿色),以及可以代表开发最成功治疗方案的潜在靶点(蓝色)。小写字母“ i”表示“抑制剂”;小写字母“ a”表示“激动剂”。
胶质母细胞瘤的免疫疗法
图6
图6概述了目前正在开发的用于治疗胶质母细胞瘤的不同免疫治疗方法,其中,包括依赖树突状细胞(DC)介导的胶质细胞瘤相关抗原的疫苗治疗;基于单克隆抗体的免疫检查点阻断药物;靶向肿瘤相关抗原的嵌合抗原受体(CAR)T细胞疗法;以及可在肿瘤细胞中选择性复制并诱导抗肿瘤免疫力病毒的溶瘤病毒疗法。
肿瘤免疫表型分析工具
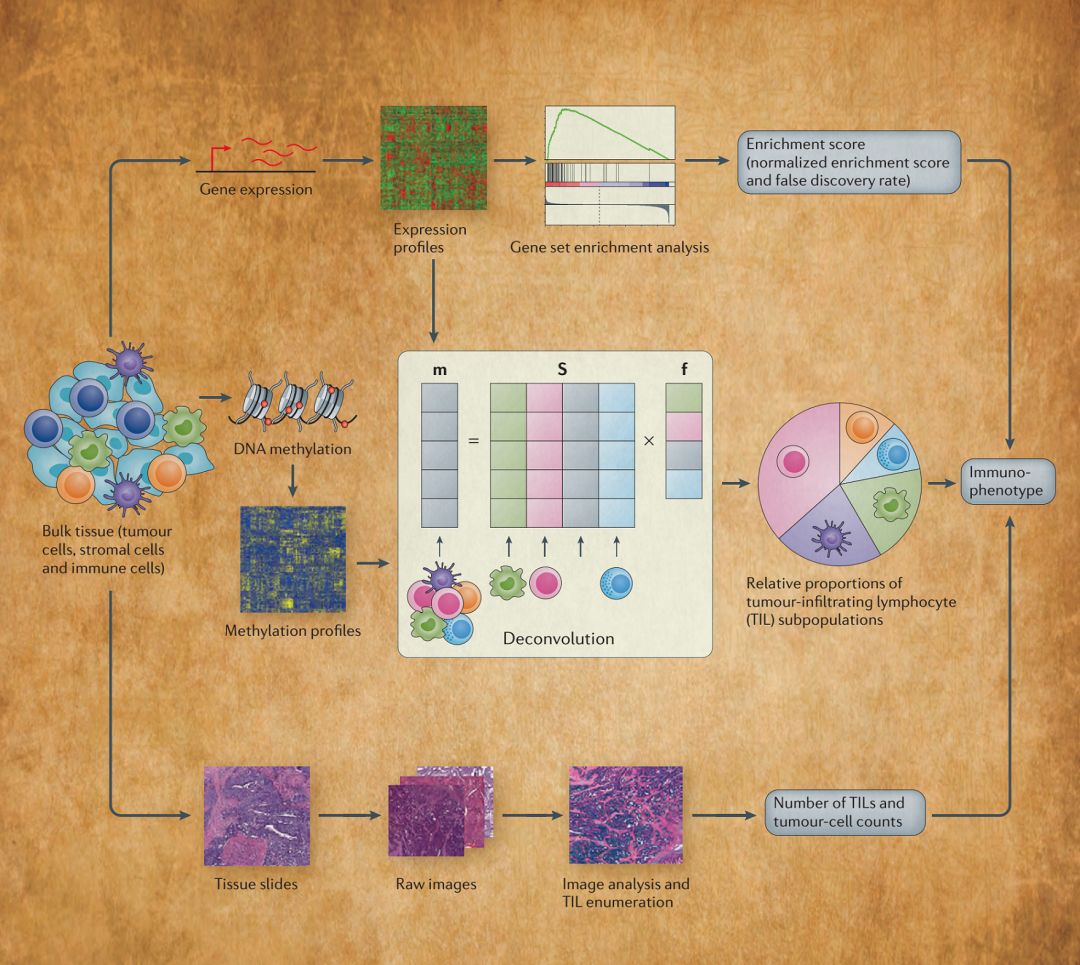
图7
图7描述了基因表达谱、DNA甲基化谱和免疫组织化学等分子信息的多种来源和可用于研究肿瘤免疫表型的计算工具。
联合疗法的基本靶点
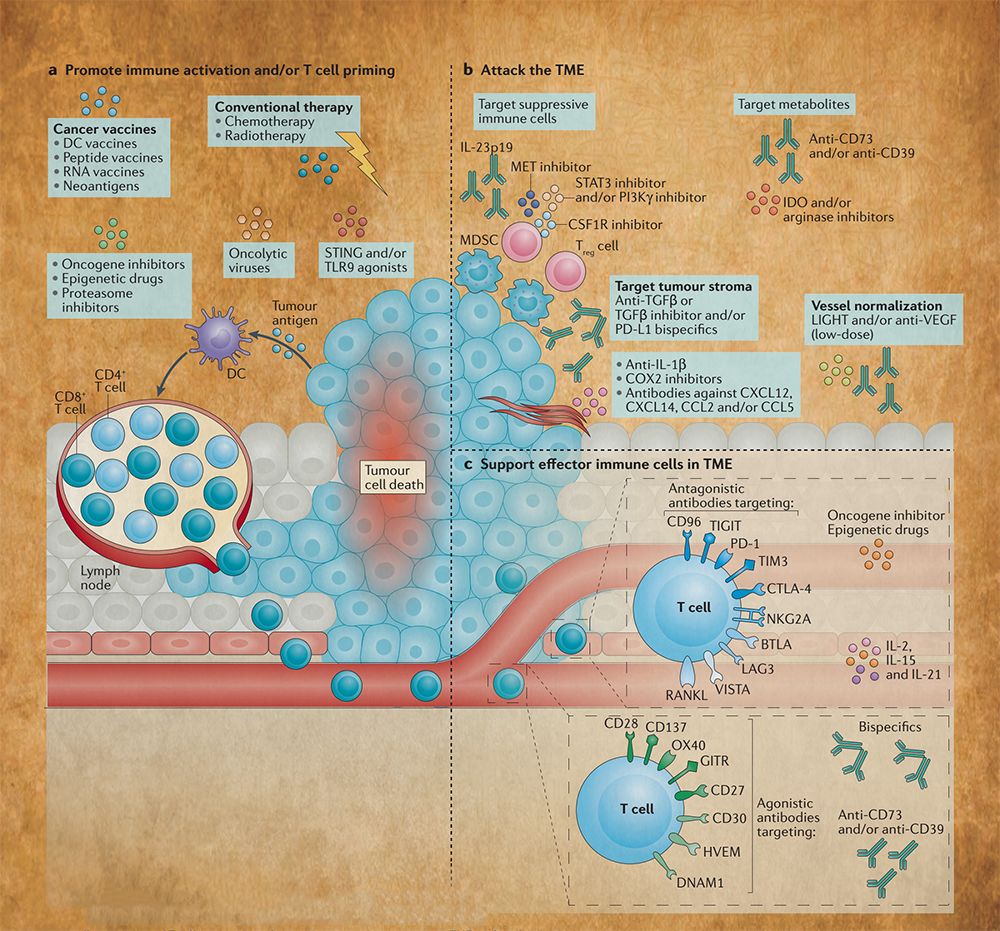
图8
图8描述了联合疗法在防止获得耐药性方面的潜力。协同作用的基本机制包括促进免疫细胞活化和T细胞启动(a);缓解肿瘤微环境(TME)诱导的免疫抑制(b);并支持TME中免疫细胞的效应器功能(c)。
膀胱癌的T细胞反应
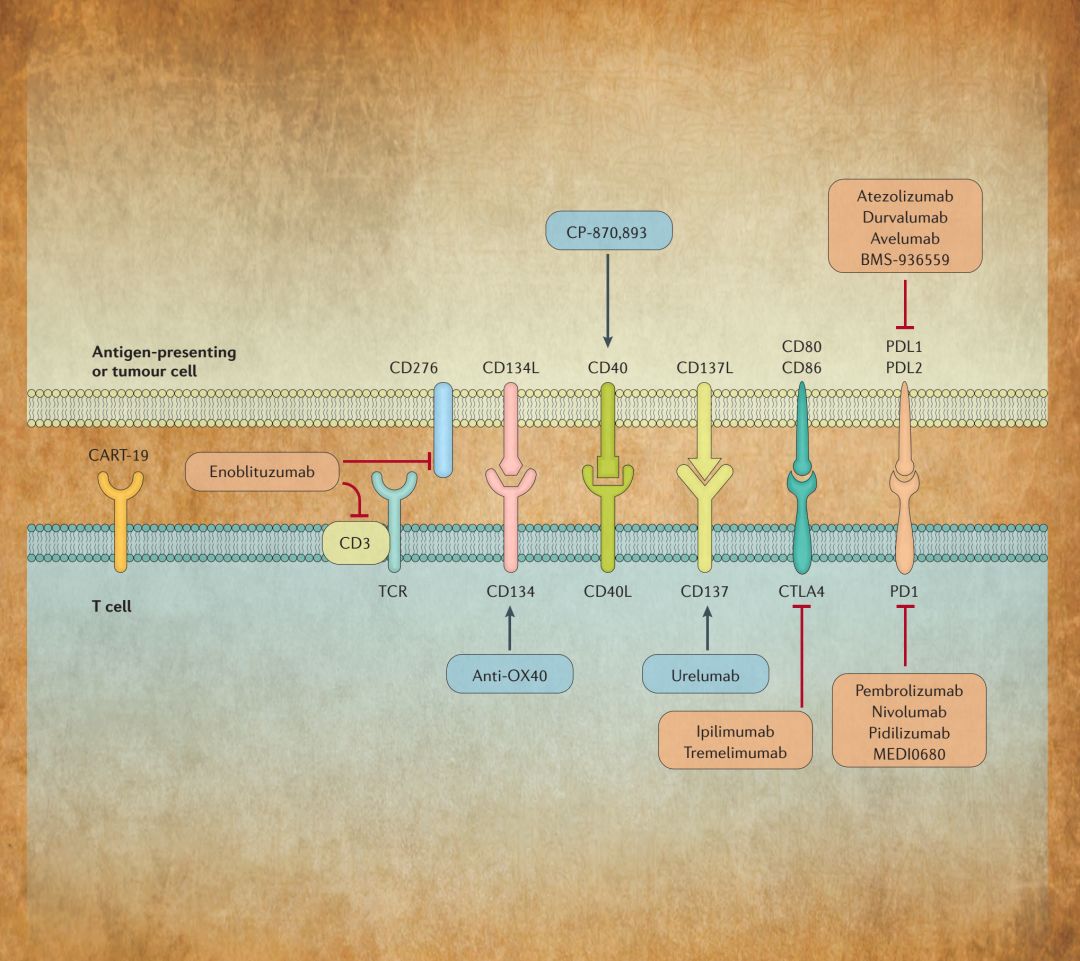
图9
图9概述了膀胱癌中T细胞与抗原呈递或癌细胞之间的各种配体-受体相互作用,这种作用可调节抗原对T细胞反应,并代表增强T细胞反应和促进免疫系统介导的癌细胞杀伤的潜在免疫治疗靶点。
靶向免疫疗法使用的生物材料
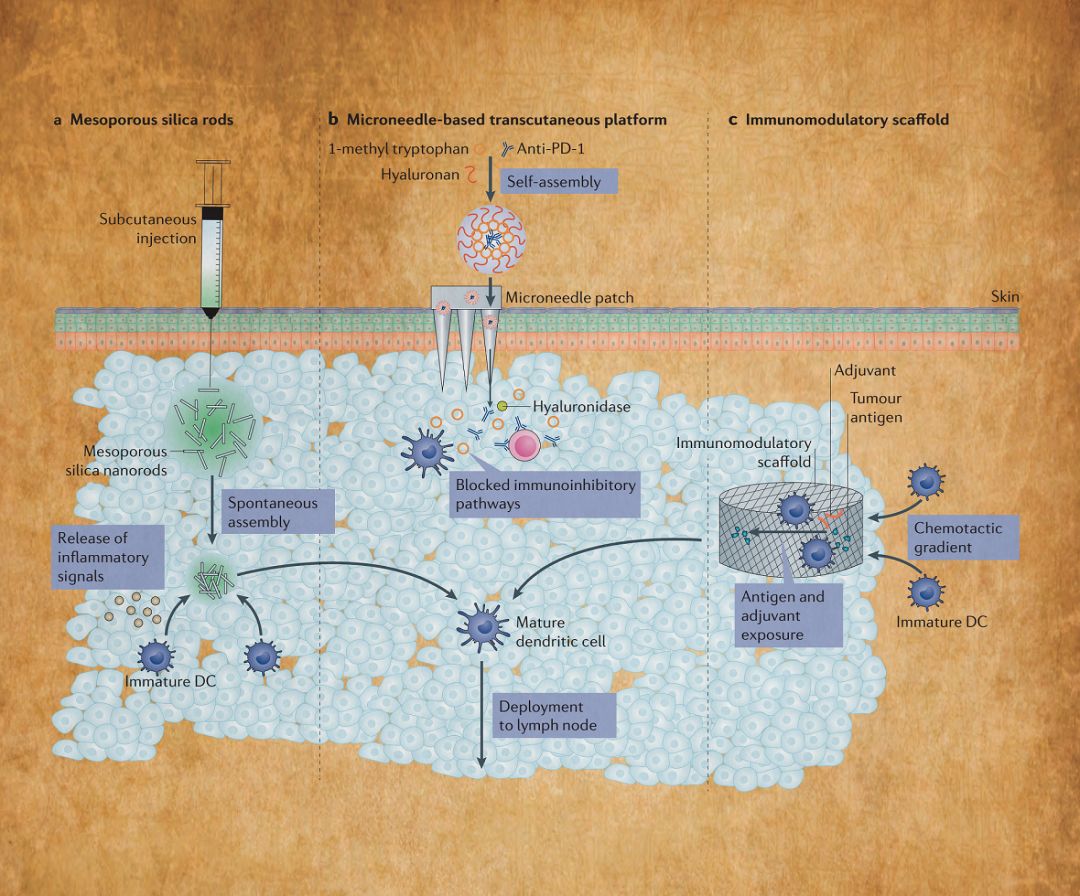
图10
科学家正在探索一些生物材料和方法来实现癌症免疫疗法的局部递送。在图10左侧,介孔二氧化硅棒在体内自发组装并募集宿主细胞使其成熟。在图片中部,基于微针的带有自组装免疫治疗纳米载体的经皮给药平台,可用于治疗药物的传递。图片右侧描绘了可皮下递送的多孔生物材料支架,该支架可释放化学吸引剂并将幼稚树突状细胞(DC)募集到其空隙,引起主要组织相容性复合物(MHC)-肽复合物中的肽呈递增加。
癌症溶瘤病毒疗法的障碍
图11
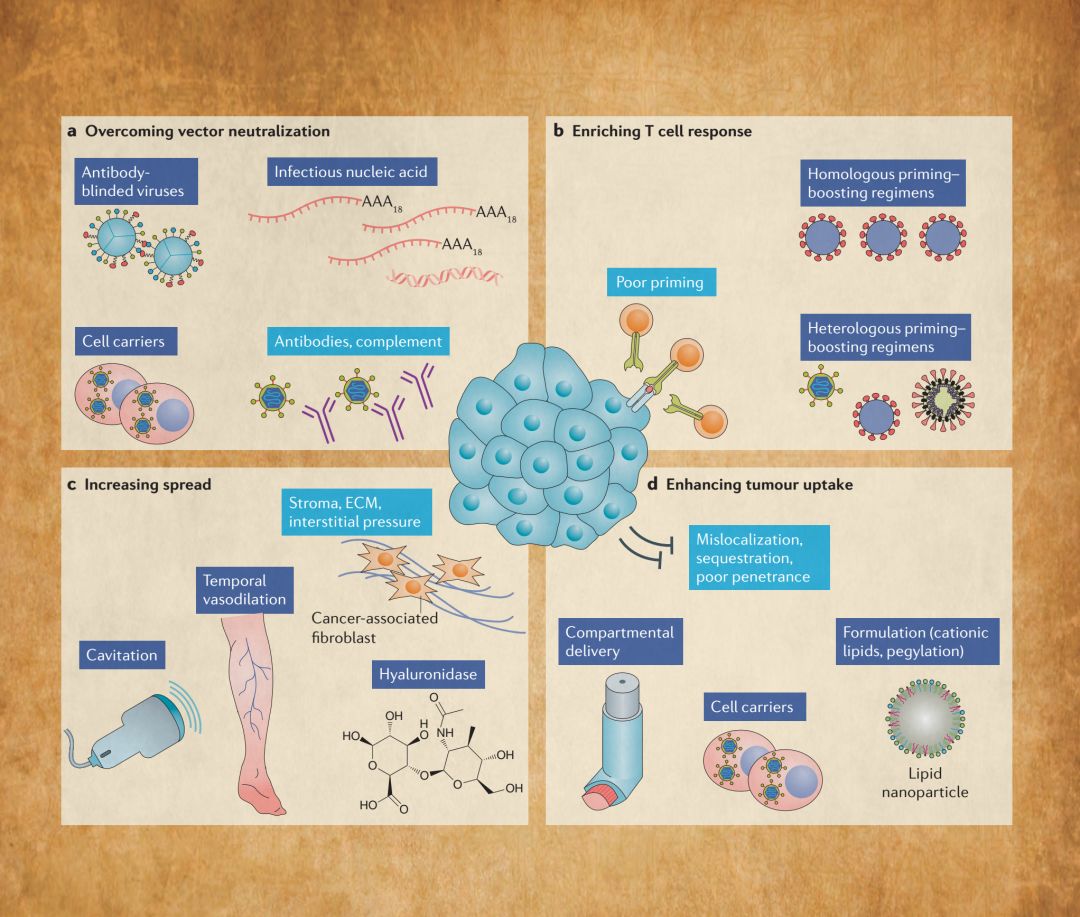
图11描述了限制溶瘤病毒(OVs)临床益处的障碍(浅蓝色)。为了优化治疗反应,可以采取生物工程、分子和免疫学方法(深蓝色)以达到以下目的:避免病毒载体被对应的抗体中和;对肿瘤细胞以外的其他类型细胞隔离OVs,增强肿瘤细胞的吸收;通过细胞外基质(ECM)增强OVs扩散;增强T细胞对肿瘤抗原的反应。
癌症新抗原的鉴定
图12
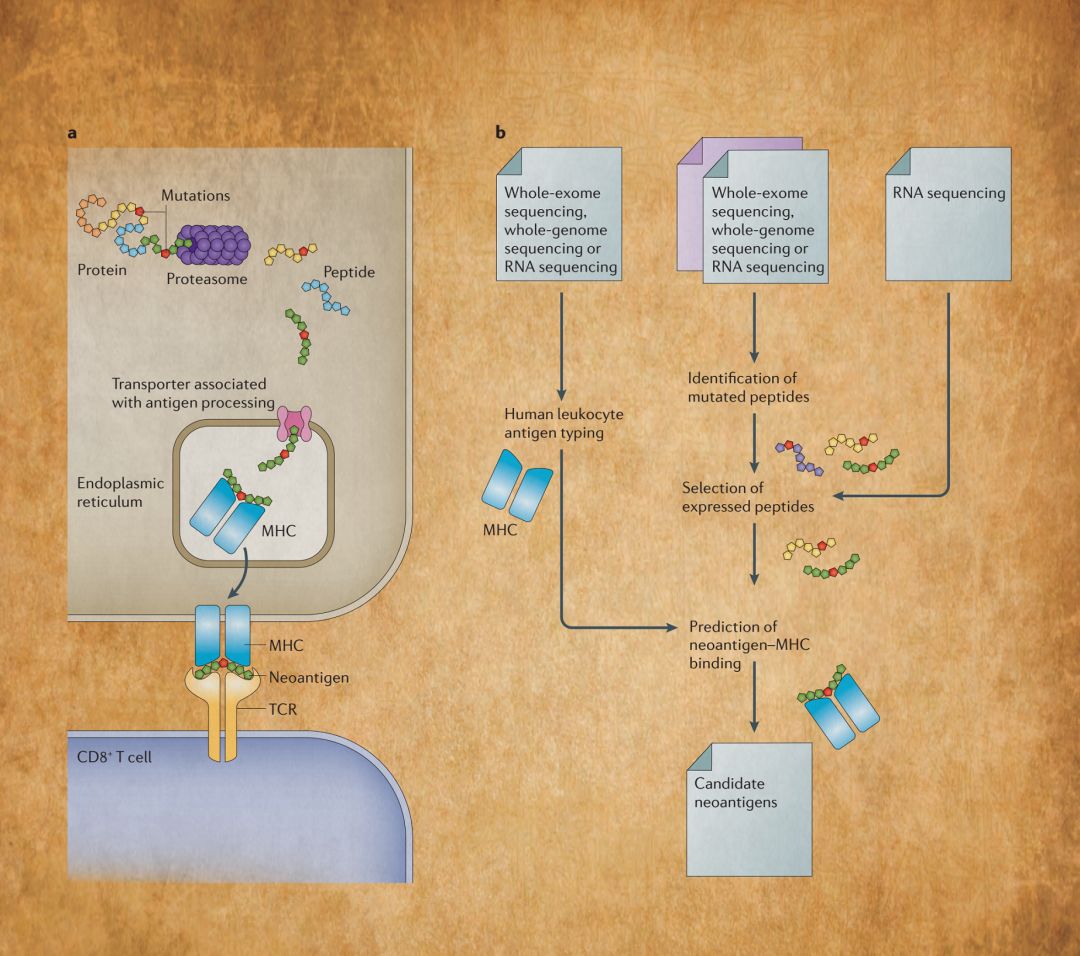
图12描绘了新抗原起源于癌细胞表达的突变蛋白,显示在抗原呈递细胞表面,并被CD8 + T细胞的TCR识别的过程(a);以及从下一代测序数据中预测候选新抗原的计算框架(b)。
嵌合抗原受体T细胞疗法(CAR-T疗法)
图13
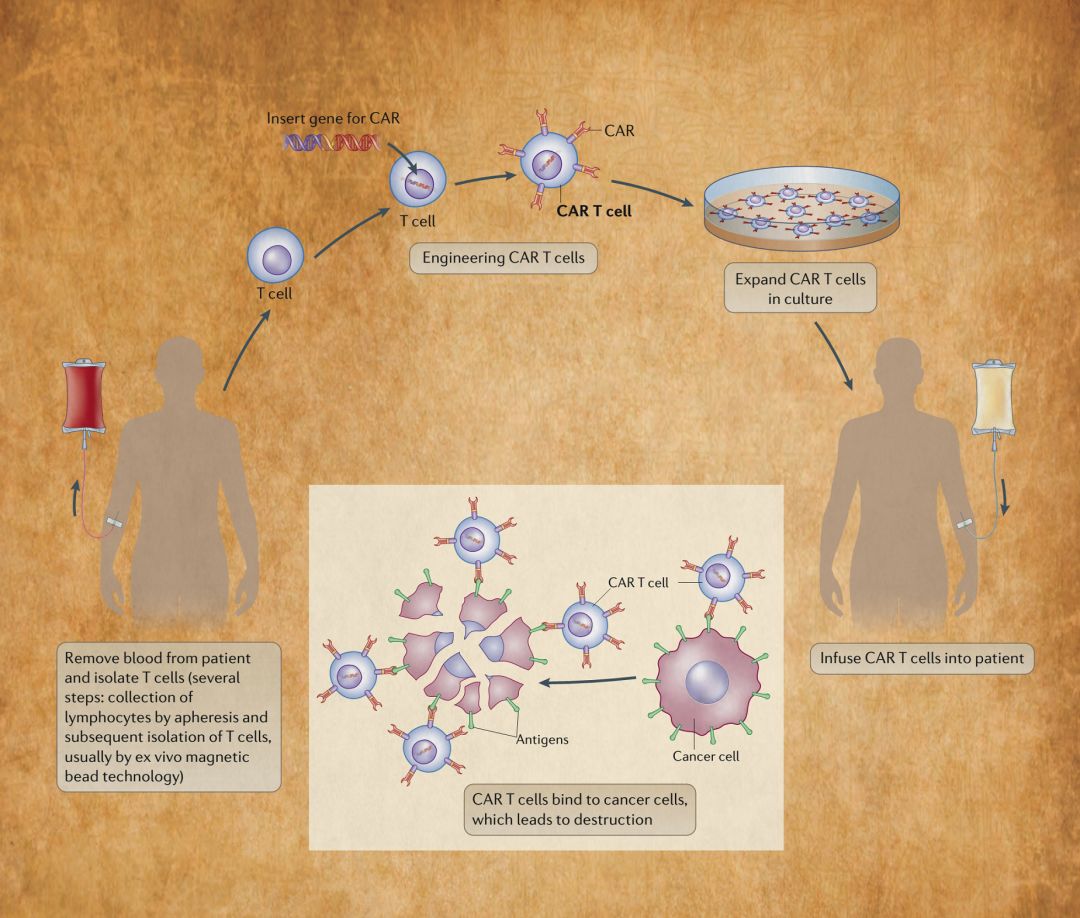
图13概述了嵌合抗原受体(CAR)T细胞疗法。从患者外周血中分离出CAR-T细胞,然后使用病毒或非病毒载体将编码CAR的基因插入到T细胞的基因组中。将工程化的T细胞在细胞培养物中增殖,然后重新注入患者体内。工程化T细胞表达的CAR将识别肿瘤细胞表面的抗原,进而激活T细胞,靶向消灭肿瘤细胞。