在多细胞动物的发育过程中,TP53基因家族已经进化了6亿到8亿年。40年前TP53被发现,在人类癌症中存在广泛突变。
P53家族
人类p53样转录因子家族有三个基因TP53、TP63和TP73。
p53、p63和p73的蛋白质结构域相似,三个DNA结合结构域几乎相同,与相似的DNA特异性序列结合,调节一些相同基因和一些不同基因的转录。
C端结构域在大小、序列和功能上各不相同,调节DNA结合和转录,介导蛋白相互作用,所有三种蛋白质的N末端序列至少编码两个不同的转录激活结构域 。
与p53相似,p63通常通过诱导细胞死亡对DNA损伤作出反应。在全身鳞状细胞上皮的产生和再生中,p63也是一个关键的转录因子,作用于颅骨、面部、四肢和中枢神经系统。
纤毛上皮细胞的产生需要p73,因此在含有这些细胞的许多组织中p73起着重要作用,如雄性生殖细胞、免疫系统、听力系统、气管、肺、中枢神经系统等。
Tp53进化
漫长进化过程中,p53、p63和p73蛋白DNA结合结构域的氨基酸序列和结构被保存下来,并被用来追踪p53家族成员在动物中的起源和进化。目前鞭毛虫含有p53同源物,其DNA结合结构域和C端与人p53的DNA结合结构域和C端非常相似,鞭毛虫可能和人类有共同祖先,估计在6亿至8亿年前就生活过。
p53激活
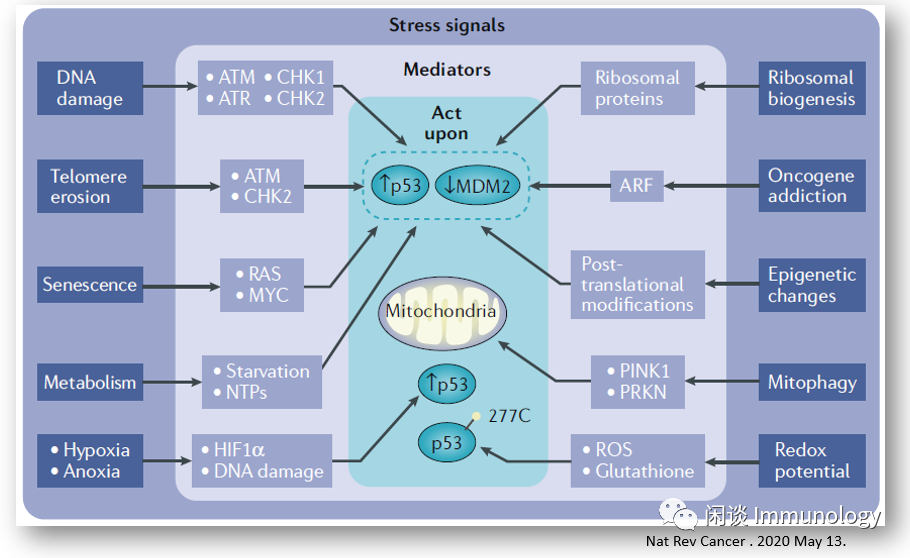
各种内在和外在的应激信号,由信号转导通路MDM2-p53节点通信的蛋白质介导的,从而导致p53转录因子的增加和激活。
至少有10种不同的应激信号通过特定的蛋白质,来调节E3泛素连接酶MDM2的活性,MDM2的激活导致p53的泛素化和蛋白酶体降解。通过MDM2泛素连接酶,p53蛋白在各种细胞中的半衰期很短,从6到40分钟不等。MDM2降解或失活,可以增加p53的半衰期。
这些信号在几分钟内迅速发生,稳定的p53蛋白,通过蛋白质-蛋白质相互作用(这是一个快速反应)和转录选定的基因(这是一个相对缓慢的反应)发挥作用。不同的应激信号在其转录方案中似乎有不同的反应, 从而对应激产生较慢的反应。
P53抑制
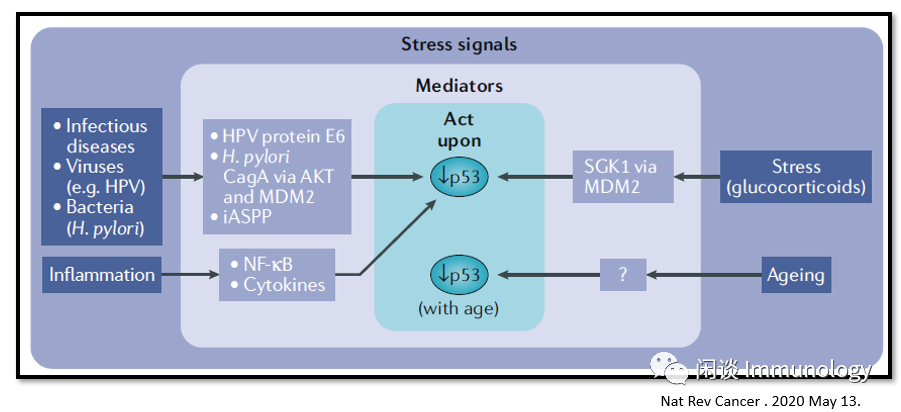
蛋白质介导的一些内在和外在的应激信号,导致细胞中p53水平降低,至少有四种类型的应激信号:传染病、炎症、皮质醇相关的心理应激(糖皮质激素)和衰老,与细胞或组织中p53的表达和/或活性降低有关,导致p53通路和应激反应的损害或失活。
P53转录
为了响应特定的应激或应激组合,细胞可以激活p53信号,介导基因转录,其蛋白质产物参与一系列下游细胞信号活动,以及参与正或负调节p53和/或p53依赖转录的基因,导致下游反应以及反馈回路。
p53激活受应激、细胞类型、表观遗传标记和应激组合(称为高阶整合)的影响,并启动转录程序,修复应激造成的损伤或以过度损伤杀死细胞。
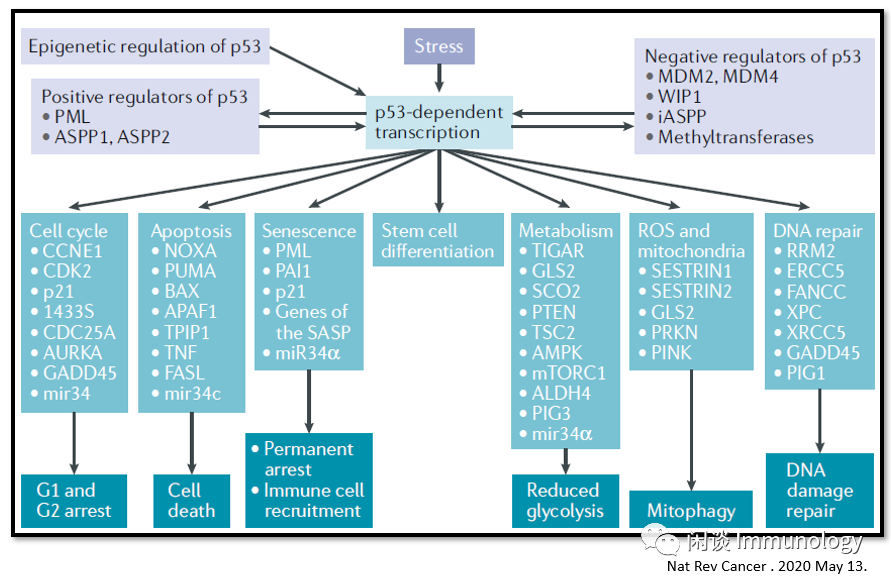
在接受应激,表观遗传改变,正负调节信号之后,p53转录激活,进而调控细胞周期,凋亡,衰老,干细胞分化,代谢(降低糖合成),ROS和线粒体,DNA损伤修复等。
p53突变
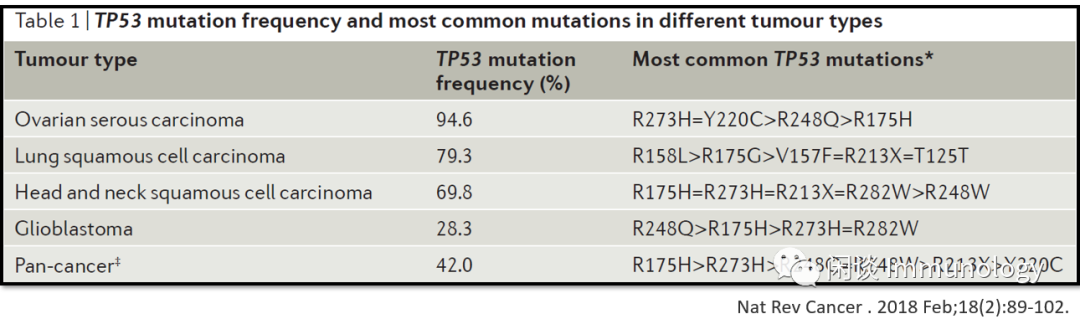
@p53肿瘤中突变频率及常见突变位点
除TP53R213x和TP53T125T外,其他TP53突变都是错义突变,在p53的DNA结合核心结构域中产生单个氨基酸替换。
TP53R213x是最常见的无义突变,TP53T125T突变不会改变氨基酸,但会影响剪接。
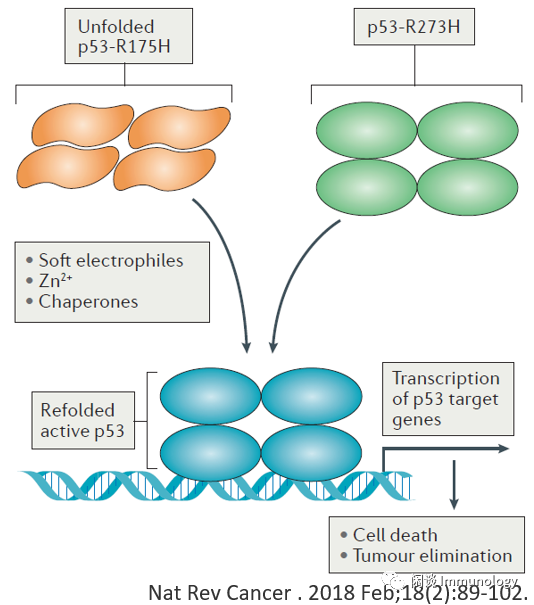
@错义突变p53的再折叠和再激活
部分或严重展开错义突变的p53蛋白(例如,p53-R175h)或错义突变的p53蛋白,其残基的替换与DNA(例如,p53-r273h)无法结合,无法调节p53靶基因的转录。由软亲电分子、伴侣或Zn2介导的突变体P53的再折叠,恢复了p53靶点的特异性DNA结合和调控,导致p53依赖的凋亡、衰老、或代谢调控,最终消除肿瘤。p53作为四聚体与DNA结合。其他再激活机制可适用于DNA接触突变体,如p53-R273h。
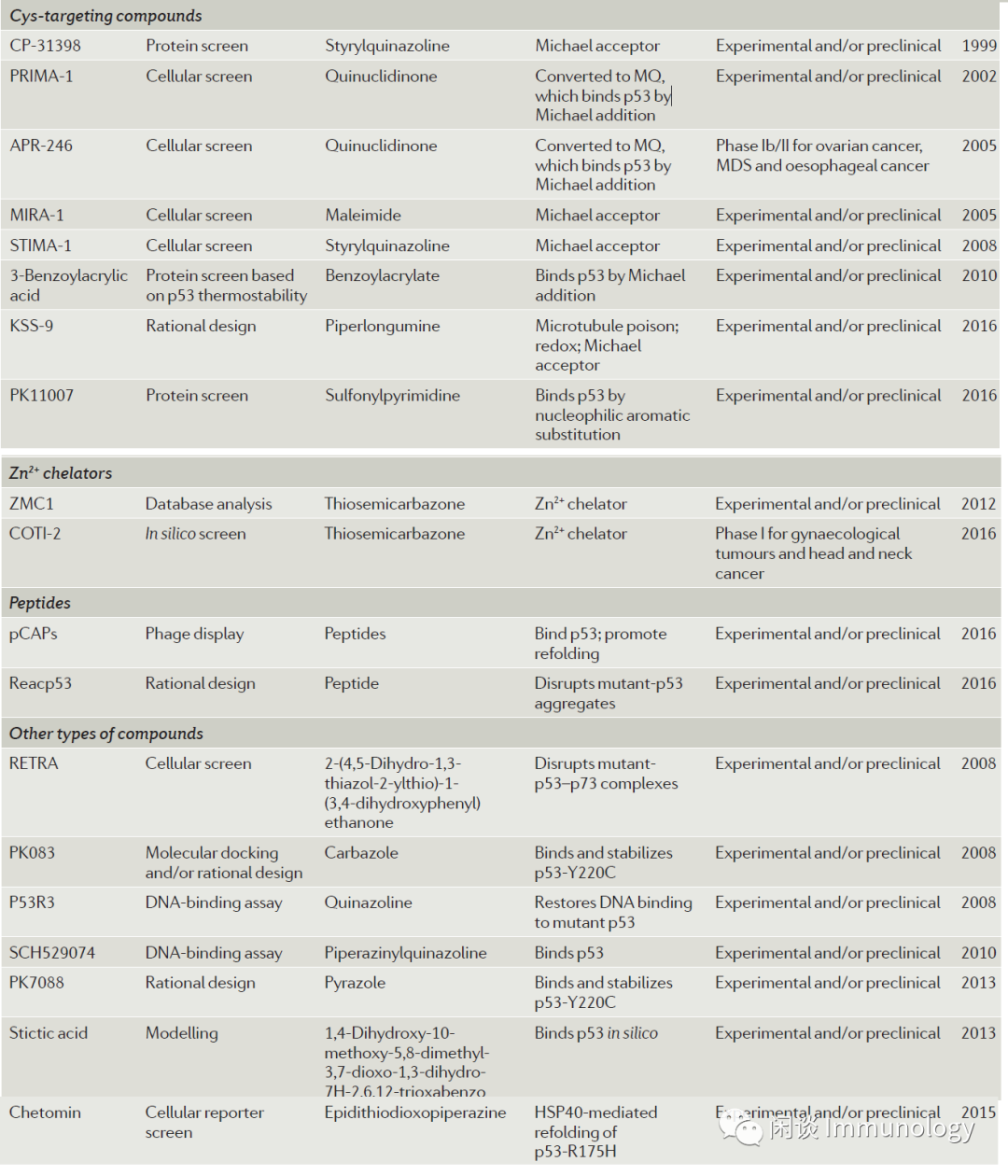
但是针对p53的药物基本在实验和临床前阶段。如下表供参考。
喵评:很多机制影响着p53靶向分子的成药性,到目前只有两个分子进临床。对这个古老的蛋白,未来可能会有新的发现。