上海2023年1月6日 /美通社/ -- 2023年1月5日,勃林格殷格翰宣布,其在研创新药物MDM2-p53拮抗剂BI 907828用于一线治疗去分化脂肪肉瘤(DDLPS)Ⅱ/Ⅲ期临床试验Brightline-1(登记号:CTR20222584),在四川大学华西医院成功入组首例DDLPS患者。Brightline-1是一项随机、开放标签、全球多中心的Ⅱ/Ⅲ期临床试验,旨在比较BI 907828与多柔比星在晚期DDLPS患者中作为一线治疗的有效性与安全性,该研究中国主要研究者(leading PI)是中山大学肿瘤防治中心张星教授。
“被遗忘的癌症”——肉瘤正面临重重困境
肉瘤是一种罕见的恶性肿瘤,发生于结缔组织,例如骨、软骨、肌肉、神经、血管以及脂肪和纤维组织,约占全球所有癌症的1%[1] 。87.3%的肉瘤发生于软组织中,如肌肉、神经、血管、脂肪和纤维组织,这些被称为软组织肉瘤(soft tissue sarcoma,STS),其亚型众多,脂肪肉瘤(liposarcoma,LPS)是最常见的亚型之一;另外12.7%的肉瘤为骨肉瘤,多起源于骨骼,也可起源于软骨[2 ]。根据美国国家癌症研究所(NCI)的SEER数据库统计,肉瘤每年的总发病率不到5/10万。
由于肉瘤的罕见性以及临床医生对该病的认知不足,延误了准确诊断以及后续的规范治疗。大多数肉瘤患者被诊断时,疾病已经处于晚期,而对应治疗方案极为匮乏——化疗是近50年来的主要治疗方法。而去分化脂肪肉瘤(DDLPS)是高侵袭性的LPS亚型,其复发率高达40%-75%,转移率为10%-15%,显著高于其它LPS亚型临床结局较差。同时,DDLPS化疗效果较差,这些患者迫切需要更加有效且毒性更小的治疗方案。
MDM2-p53拮抗剂BI 907828是一种口服小分子化合物,可抑制MDM2和p53蛋白之间的相互作用。P53是一种驱动肿瘤细胞死亡的肿瘤抑制因子,而MDM2是p53的主要负调控因子,可以与p53结合并促进其清除,并且MDM2基因扩增是DDLPS中最为常见的基因改变,在90%的DDLPS病例中存在,为BI 907828在DDLPS中的广泛应用奠定了基础。
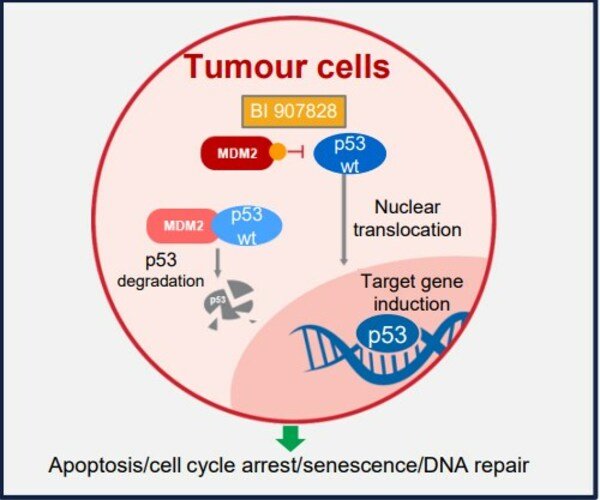
BI 907828作用机制示意图
BI 907828有望变革由MDM2-p53轴突变驱动的癌症患者治疗
BI 907828已经在DDLPS的治疗中展现了初步潜力,2022欧洲内科肿瘤学会(ESMO)大会上,BI 907828治疗TP53野生型、MDM2-扩增实体瘤患者的剂量扩展Ⅰb期研究数据显示,BI 907828对DDLPS的疾病控制率(DCR)为93%,其中2例达到部分缓解(PR),5例DDLPS患者的无进展生存期(PFS)>10.5个月,并且不良反应安全可控[3] 。
中山大学肿瘤防治中心张星教授表示:“BI 907828 Ⅱ/Ⅲ期临床试验的正式启动意义重大,给中国DDLPS患者带来了新的希望,使得这部分罕见瘤种的患者能够在第一时间接触到首创/突破性的治疗手段和药物。此外,借助勃林格殷格翰的临床研究合作项目,让中国临床研究者能够与全球接轨‘零时差’开展研发计划与临床试验,这对我国药物临床研究的促进意义也不言而喻——在提升中国研究者临床研究能力的同时,也积极推动中国的试验进展,让更多中国DDLPS患者早日用上创新药。”
四川大学华西医院姜愚教授谈到:“DDLPS患者长久以来缺乏有效的治疗手段,而BI 907828的出现无疑为这部分患者打开了一扇‘新大门’。BI 907828在Ⅰb期试验中已经展现出了令人鼓舞的治疗潜力,而此次首例患者成功在我院入组,标志着中国患者能够更早地从创新药物中获益,中国患者的需求能够更早地在研发计划中体现,中国数据能够在第一时间应用于临床,我很期待BI 907828能为更多患者带来临床获益。”
勃林格殷格翰中国医学和研发负责人张维博士表示:“我们很欣喜看到BI 907828 Ⅱ/Ⅲ期临床试验取得阶段性进展,在中国成功入组首例患者。BI 907828的早期疗效数据已经展现出了一定潜力,基于循证医学证据以及临床需求,美国食品药品监督管理局(FDA)已经授予BI 907828孤儿药认定资格,用于治疗软组织肉瘤,包括DDLPS。得益于‘中国关键(China Key)’项目的深入开展,使得中国患者、中国研究者、中国治疗中心能够参与全球性早期研究,此次Brightline-1研究也正是‘中国关键’项目的又一延伸。基于‘Winning in Oncology’的全球策略,勃林格殷格翰目前正积极布局肿瘤药物管线,不断优化现有肿瘤治疗方式并努力开发创新疗法,同时希望能够与中国研究者们共同努力加速试验进展,最终将试验成果惠及到全球患者。”






