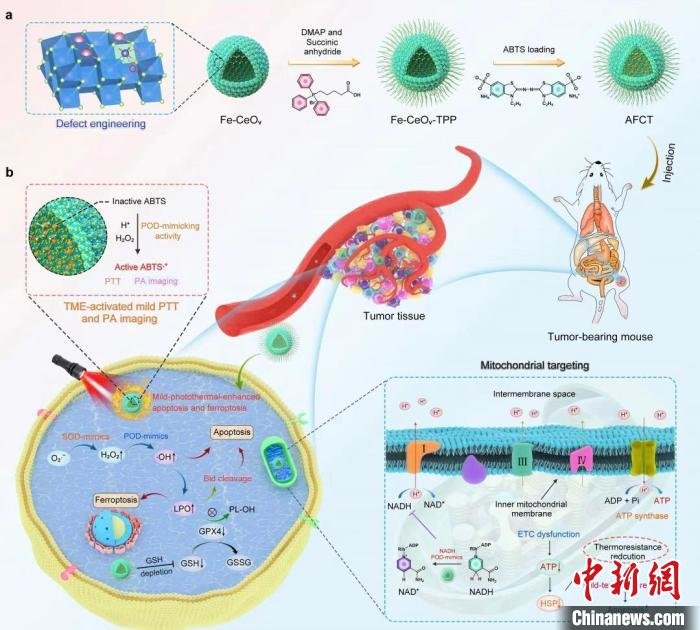
纳米酶的合成及肿瘤微环境特异性激活的协同抗癌机理示意图 哈工程提供
中新网哈尔滨4月11日电 (刘菊蓉)哈尔滨工程大学11日发布消息,该校材料科学与化学工程学院盖世丽教授及所在无机功能材料应用基础研究团队提出了一种癌症光热疗法疗效提升新策略,为纳米材料在医学领域内的应用提供了重要的理论基础。
光热疗法作为一种新型癌症治疗手段,将具有较高光热转换效率的材料注射入人体内部,利用靶向性识别技术聚集在肿瘤组织附近,在外部光源的照射下将光能转化为热能,以最小的侵入性和高精确性杀死癌细胞,已成为癌症诊断和治疗的潜在对策。
在临床应用中,传统光能转化材料存在热扩散引起健康组织热损伤、热休克反应加剧肿瘤细胞热耐性、非特异性光热引起生物安全问题、单一疗法效率不足等风险。盖世丽及所在团队结合抗癌治疗新武器“纳米酶”,引入一种“电子传输链干扰和协同辅助治疗”的策略。
哈尔滨工程大学材化学院盖世丽教授 哈工程提供
在正常的生理环境下,该纳米酶就像是合上的“锁”,只有在响应肿瘤微环境过氧化氢和弱酸性两把“钥匙”的驱动下,纳米酶的光热和成像功能会被特异性地激活,大大减少了对正常细胞的伤害,有效避免副作用。
同时通过表面功能化三苯基膦分子,为纳米酶装上“导航”,使其精准定位到肿瘤细胞的线粒体,通过“电子传输链”策略,下调肿瘤细胞中的热休克蛋白,进而缓解肿瘤细胞耐热性。这一研究克服了传统光热治疗的多种局限,实现了有效的肿瘤特异性的协同温和光热及纳米催化治疗。
相关研究成果对实现具有多类酶催化性质的纳米生物材料的设计制备、肿瘤光热治疗疗效提升等医学领域内的应用具有重要的指导意义,有望为肿瘤的治疗提供新方法,促进中国相关生物医用材料发展水平。
相关成果以“‘ETC’策略增强的光热与缺陷工程促进的多酶活性协同个性化抑制肿瘤生长”为题发表在化学领域顶级期刊《美国化学会志》(Journal of the American Chemical Society, JACS)上,并被选为封面文章。(完)


