"
最新全球数据汇总分析显示,CTC计数可强烈预测转移性乳腺癌患者的总体生存结果。CTC持续阴性患者的mOS可达47.05个月,而在CTC持续阳性的患者中,mOS则为17.87个月。
"
CTC,循环肿瘤细胞(Circulating Tumor Cell),即肿瘤因自发生长或因诊疗操作进入血液循环中的各类肿瘤细胞总称。 CTC具有血行转移、免疫逃逸、自我种植等特征,是导致肿瘤扩散的关键因素。
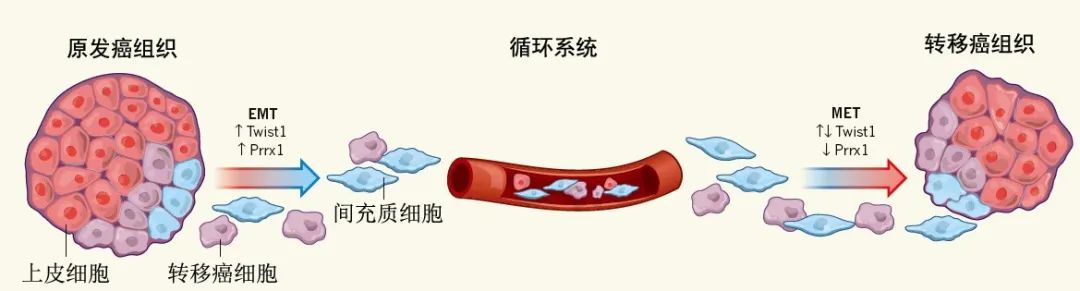
▲ CTC转移过程
晚期肿瘤每天会释放数百万个肿瘤细胞进入循环系统,但这些肿瘤细胞的半衰期很短,只有极小一部分会形成转移灶。可以想象,当CTC停留在一个器官的毛细血管床上,而恰巧这个器官又提供了有利的生长微环境,那么CTC就可能会穿过血管形成新的转移灶。原发肿瘤体积越大,这一过程发生的可能性就越大。所以,通过CTC检测理论上是可以进行肿瘤的动态监测和预后判断的。
2020年12月11日,圣安东尼奥乳腺癌研讨会(SABCS)线上举办,会议期间公布了一项全球性“关于循环肿瘤细胞(CTC)计数预测转移性乳腺癌(MBC)预后和疗效的14个临床试验的合并分析”结果,结果显示:在治疗开始后第29天(26-54天),连续对CTC进行评估可以有效预测转移性乳腺癌的总生存期(OS)。
这是迄今为止最大的有关连续CTC计数在MBC早期治疗监测的合并分析,它包含了个体患者的数据。这项研究的重点是在不同乳腺癌亚型中CTC对OS的预测能力!
这是一项国际合作的汇总分析,包括在亚洲,欧洲和北美进行的前所未有的多机构临床试验 。研究人员从经过同行评审文献中发表的前瞻性临床研究获得身份不明的个体患者水平数据,以生成4,079名参与者的数据集,从而进一步定义和验证CTC计数在早期监测转移性乳腺癌患者状态中的作用,而不考虑HR和HER2亚型状态。
▲ 14项临床研究的4,000余名参与者
合并分析的数据分别在患者基线时和开始治疗后29天(中位数,26-54天)开始收集,使用的是液体活检先驱 Menarini Silicon Biosystems的CellSearch® CTC系统对所有患者血液中CTC进行检测,捕获,分离和表型分析。
CellSearch是第一个也是唯一一个经过临床验证的CTC检测系统,该系统已获FDA/NMPA批准用于转移性乳腺癌(NMPA)、前列腺癌和结直肠癌患者中CTC的鉴定,分离和计数。
检测原理:CellSearch检测试剂盒包含一种基于铁磁流体的捕获试剂和免疫荧光试剂;这种铁磁流体试剂含有带磁芯的纳米颗粒,在磁芯周围的聚合物层上涂覆有针对EpCAM抗原的抗体,以捕获CTC。在免疫磁珠体完成了捕获并富集之后,添加荧光试剂以识别并计数CTC。荧光试剂中包括:专用于细胞角蛋白的抗CK藻红素(PE),对细胞核染色的DAPI,以及专用于白细胞的抗CD45藻蓝蛋白(APC)。如果它的形态特征与肿瘤细胞的相一致,并且免疫分型 EpCAM+、CK+、DAPI+和CD45-,则将它归类为肿瘤细胞。
为了观察连续CTC计数在MBC早期治疗监测中的作用,研究人员根据基线时的CTC状态和随访情况(中位29天)将患者分为4组(研究人员将CTC阳性定义为可检测到的CTC≥1):
1. CTC阴性/阴性或持续阴性(19.9%);
2. CTC阴性/阳性(7.5%);
3. CTC阳性/阴性(27.1%);
4. CTC阳性/阳性或持续阳性(45.5%)。
结果采用常用的对数秩和Cox回归检验进行分析,这些统计分析的重点是全患者队列和定义亚组中连续CTC计数结果与总生存期(OS)之间的关系。亚组包括HR+型,HER2型,三阴性及未明确乳腺癌类型的转移性乳腺癌患者。
研究结果显示,所有组在基线和随访时(中位29天):
1. CTC持续阴性,中位OS为47.5个月;
2. CTC持续阳性,中位OS仅有17.87个月;
3. CTC阴性/阳性,中位OS为29.67个月;
4. CTC阳性/阴性,中位OS为32.20个月。
3和4这两组无显著差异,不过CTC从阴性转变为阳性时,危险增加了74%,CTC从阳性转变为阴性时,死亡率比CTC持续阳性降低了51%。此外,用CTC≥1个或≥5个的cut-off值进行分析时,亦产生了相似的结果。
此外,研究人员根据乳腺癌的亚型分析了结果,在三个主要亚型中,结果相似。与CTC持续阳性相比,管腔乳腺癌患者的死亡率从阳性转变为阴性的危险减少了53%,HER2乳腺癌患者的危险减少了46%,三阴性乳腺癌患者的危险减少了59%。
这是一个非常大的汇总分析,真正向我们提供了一种非侵入性的液体活检方法,该方法可能比传统的影像方法具有优势,而传统的影像方法可能需要长达3个月的时间才能在乳腺肿瘤中检测到变化。CTC的监测可以作为晚期乳腺癌早期治疗反应的指标,具有潜在的临床应用价值。
1.Janni W, Yab C, Hayes DF, et al. Clinical utility of serial circulating tumor cell (CTC) enumeration as early treatment monitoring tool in metastatic breast cancer (MBC) – a global pooled analysis with individual patient data. Presented at: 2020 San Antonio Breast Cancer Symposium; December 8-11, 2020; virtual. Abstract GS4-08.