细胞有丝分裂错误和DNA损伤会导致造血干细胞(HSC)的DNA发生基因突变,并逐渐积累。在这个过程中,某些特定的细胞群会获得优势性扩增,这种现象称为克隆性造血(clonal haematopoiesis,CH)。克隆性造血会增加个体血液肿瘤、细胞减少、心血管疾病(CVD)和感染的患病风险。因此,克隆性造血可以提高我们对这些常见疾病发展中启动事件的理解。
近日,美国再生元遗传研究中心研究团队,利用628,388个个体的全外显子组序列数据识别了40,208个意义不明克隆性造血(CHIP)的携带者。经过全基因组和全外显子组关联分析,鉴定了24个位点(21个为新位点),发现其中胚系遗传变异影响CHIP的易感性,并确定了与克隆性造血和端粒长度相关的新型罕见变异。研究分析了特定CHIP基因突变携带者中发生癌症、CVD和全因死亡率的风险,并使用孟德尔随机化验证了CHIP与目标表型之间因果关系的证据。最终结果表明,CHIP代表了一组复杂的异质表型,具有共同和独特的胚系遗传因素以及不同的临床意义。该研究发表在Nature上,文章题为“Common and rare variant associations with clonal haematopoiesis phenotypes”。

文章发表在Nature上
主要研究内容及结果
研究人员使用来自UKB中CHIP突变携带者的遗传信息进行共变异全基因组关联研究(GWAS)和基因负荷外显子组关联研究(ExWAS)。使用来自GHS队列的CHIP突变携带者进行重复分析。为了鉴定特定克隆性造血驱动突变的胚系预测因子,研究团队还在单个CHIP基因突变携带者中进行GWAS和ExWAS。最后将CHIP的遗传关联结果与血液中体细胞的其他克隆性造血表型的分析结果进行比较,包括镶嵌染色体交替(mCA)、性染色体的镶嵌缺失(mLOX,mLOY)和端粒长度。
1.与CHIP携带者状态的遗传关联
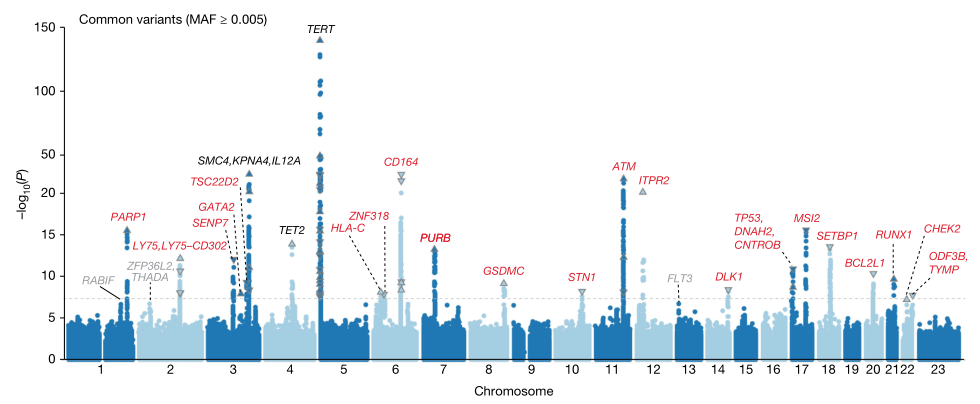
研究人员在UKB队列中进行遗传关联分析,以确定与发生CHIP风险相关的胚系位点。在常见变异GWAS中,包括25657例病例和342869名对照,研究确定了24个位点(21个新位点),包含57个独立相关变异(图1)。
图1. 克隆性造血的GWAS分析。来源:Nature
2.单个CHIP基因突变分析
在遗传关联分析中,研究团队将单个CHIP基因携带者与无CHIP对照进行了比较,并在GHS中进行验证,并发现了相关基因位点对CHIP亚型的共同、独特和相反的影响,包括8个全基因组显著基因位点,这些位点在CHIP整体分析中并不显著(图2a)。研究发现,DNMT3A是整个CHIP表型中最常见的突变基因,具有最多的显著相关位点(n=23)(图2b)。
图2. CHIP基因特异性关联分析结果。来源:Nature
3.CHIP基因与表型关联
研究人员分析了CHIP基因突变携带者表型状态。分析结果与先前的发现一致,大多数相关表型来自心血管、血液、肿瘤、感染、肾脏和吸烟等(图3)。ASXL1 CHIP与数量最多和范围最广的特征有关,其中许多关联可以追溯到吸烟的相关性。SUZ12 CHIP在CHIP基因之间显示出明显的关联特征,内分泌和眼科性状的关联比例高于其他CHIP基因。白细胞计数、血小板计数和中性粒细胞计数等均与DNMT3A CHIP呈正相关,与TET2 CHIP呈负相关(图3) 。
图3. CHIP亚型的表型关联。来源:Nature
4.CHIP与COVID-19感染之间的关联
鉴于已有报道称克隆性造血与COVID-19和其他感染的风险增加有关,研究人员在UKB队列中检测了CHIP与COVID-19感染之间的关联,发现CHIP携带者状态与COVID-19住院率和重度COVID-19感染显著相关。研究团队排除了以前患有任何血癌的个体,并根据年龄、性别、吸烟、BMI、2型糖尿病、活动性恶性肿瘤和五个遗传主要成分进行了调整。CHIP亚型水平分析表明,PPM1D携带者发生重症COVID-19的风险可能升高。
结语
克隆性造血涉及某些血细胞谱系的扩增,并与衰老和不良健康结果有关。研究团队使用全基因组和外显子组关联分析,发现胚系遗传变异影响CHIP易感性,包括淋巴细胞抗原编码基因LY75中的错义变异,这与CHIP的发生率降低有关。对英国生物银行(UKB)的5041个健康特征分析发现,CHIP与严重的COVID-19结果、心血管疾病、血液学特征、恶性肿瘤、吸烟、肥胖、感染和全因死亡率之间存在关系。
该研究发现了许多与CHIP和其他克隆性造血表型相关的常见和罕见变异,这有助于为未来的功能、机制和治疗研究奠定基础。总的来说,该分析强调,CHIP实际上是一个由体细胞突变驱动的亚型组合,具有共同的遗传因素和独特的风险特征。