作者:青栎,题图来自:视觉中国
公元前4世纪,古希腊医生希波克拉底发现了一种奇怪的疾病,患者面部就像被狼撕咬过一样,可他们却并未遭受狼的袭击,后来人们用拉丁语Lupus(狼)来描述这种疾病,起名红斑狼疮(SLE)。由于病症主要体现在患者表皮,因此人们一直将它视作为一种皮肤病。
这种疾病始终并未找到有效的治疗方法。很久之后医生才逐渐意识到,它可能并不是简单的皮肤病,而是一种因自身免疫系统异常所导致的疾病。SLE不仅会让人皮肤生疮,更会影响关节、肾脏、心脏和大脑等多个器官,甚至最终导致患者死亡。
现如今,全世界约有500万人饱受这一疾病折磨,而其中90%是女性,发病年龄仅为30岁左右,至2025年全球SLE患者总数预计将达到818万人,其中我国患者数将达到106万。这些数据不难看出,战胜SLE具有极大的社会价值,如果人类可以将其攻克,那么无疑会诞生又一爆款药物。
现实总是充满遗憾,尽管诸多大药企入局研发,但时至今日依然没有SLE特效药问世。究竟为何人类始终无法攻克红斑狼疮?哪些疗法又具备破局的可能?
一、神秘的红斑狼疮
SLE算得上是世界上最神秘的疾病之一,发病机制模糊,患者确诊难度极大。
在人类试图攻克SLE初期,曾将SLE的发病诱因归结为病毒入侵或细菌感染,但在这条道路上的长期探索却并未获得丝毫成效。直至1943年,一位名叫哈格雷的血液病专家在患者骨髓中发现了一种奇怪的细胞,巧合的是这种细胞也在SLE患者身上被发现,由此开启了人类对于SLE细胞层面的探索新纪元。
“狼疮细胞”被发现的五年后,另一位医生希克斯在实验中证实,“狼疮细胞”可以利用SLE患者的血清,由患者骨髓细胞诱导而来。这也使得业界将攻克SLE的方向进一步锁定为血清层面,而非细胞层面。
1957年,间接荧光法问世,通过这种前沿技术,业界再次发现导致“狼疮细胞”的血清球蛋白针对的是DNA和核酸组蛋白,这种针对DNA的球蛋白被命名为抗核因子,也被称为抗核抗体(ANA)。
从那时起,人类才最终确定,SLE并不是由感染所致,而是一种自身免疫性疾病。能够诱导“狼疮细胞”细胞形成的ANA也被认定为SLE早期筛查的“金标准”。
然而,虽然人们找到了SLE的诱因,但究竟这种ANA因何而生却始终是一个谜团。目前人们只能确认SLE与遗传、性激素、环境等多种因素有关,这些因素互相作用引起免疫系统出现混乱,进而引发针对皮肤、关节、血液、肾脏、大脑等不同组织的异常自身免疫反应,造成这些组织不可逆损害,最终导致患者死亡。
同样的困扰也存在于诊断层面。皮肤病变是SLE的典型特征,但当患者发现这种病变时,病情往往已经较为严重。在发病早期,SLE往往伴随的是发热、体重下降、疲倦等轻微症状,因此患者想要及早确诊SLE其实也并不容易。
二、慢病策略
鉴于SLE始终没有特效药可以根治,当前的治疗方案主要是对患者进行慢病管理,患者只能通过终身服用激素类药物来对抗“不死癌症”。
慢病管理即是对慢性非传染性疾病及其风险因素进行定期检测、连续监测、评估与综合干预管理的医学行为及过程,类似于治疗糖尿病、高血压。长期的治疗目标是降低疾病复发率,减少器官系统损害,延长患者生存时间,降低死亡率,并减轻医疗负担。
在SLE慢病管理中,需要对疾病活动度和器官损伤进行评估,根据不同的评估结果选择不同的药物,以最大限度地降低药物的副作用。在药物选择上,常规以激素药物、抗疟药物、免疫抑制剂等为主。
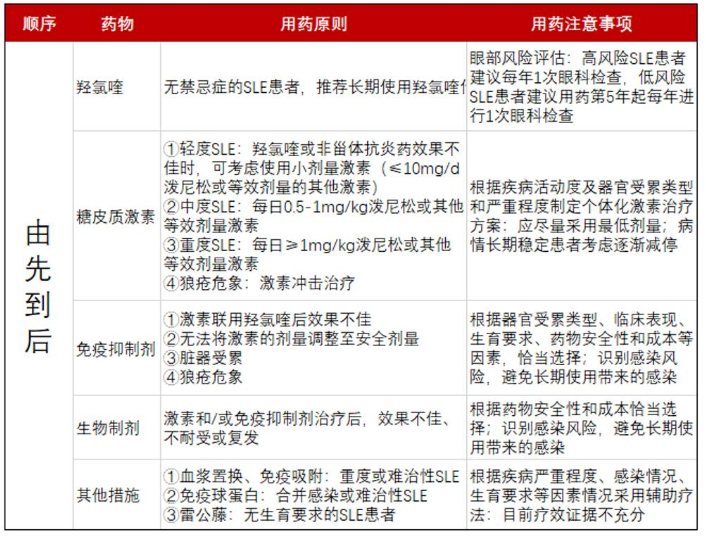
图:SLE治疗手段,来源:西部证券
糖皮质激素是SLE最常用的基础药物,能够快速抑制机体免疫状态、抗炎和抑制毛细血管的扩张,使患者的病态症状得到有效改善。常用的糖皮质激素包括氢化可的松、可的松、泼尼松、泼尼松龙、甲泼尼龙、曲安奈德、倍他米松、地塞米松等。但长期使用糖皮质激素却有诸多不良反应,例如诱发糖尿病、骨质疏松、不可逆的器官损伤、免疫功能紊乱。
抗疟药物主要是羟氯喹,能够降低疾病活动度及器官损伤风险,减少糖皮质激素使用,降低发生器官损伤和血栓的风险,从而提高患者生存率。虽然羟氯喹是一种相对安全的药物,但长期使用仍存在视网膜病变风险。
免疫抑制剂通常与糖皮质激素或羟氯喹联用,通过抑制机体异常免疫表达来控制体内细胞及体液免疫应答,减轻组织免疫损伤,从而降低患者免疫力的作用。常用的免疫抑制剂包括霉酚酸酯、环磷酰胺、来氟米特、甲氨蝶呤、环孢素、硫唑嘌呤等。
随着对SLE的科学慢病管理,患者的生存率得到极大改善,由过去急性、高致死性疾病转为慢性、可控性疾病。患者5年生存率从上世纪50年代的50%升高至90%以上。
尽管如此,可SLE巨大的研发缺口依然显著。在过去很长一段时间,关于SLE的药物研发一直停滞不前。从1955年羟氯喹被批准用于治疗SLE到2011年的50多年时间中,美国FDA都没有批准过一个治疗SLE的新药上市。
近些年,基础研究以及创新生物制剂研发蓬勃发展,具有靶向性的生物制剂成为SLE新的发展方向。科学家发现了超过100个与SLE相关的遗传易感基因位点,这些易感基因主要涉及T淋巴细胞和B淋巴细胞,是产生SLE细胞因子特征环境的重要贡献者。
尤其是SLE女性占比极高的特点,证明SLE可能与雌激素有关,许多女性在月经或怀孕期间,雌激素水平较高时,红斑狼疮症状往往更为严重。此外,紫外线、病毒感染、药物等外界因素也可能是触发红斑狼疮的原因之一。
如此背景之下,已经有多款靶向性的生物制剂获批用于治疗SLE,如GSK的贝利尤单抗、荣昌生物的泰它西普、以及阿斯利康的阿尼鲁单抗。
图:已经上市的SLE生物制剂,来源:中金公司
这些靶向性生物制剂主要通过抑制B、T淋巴细胞的活化、阻断免疫细胞间的相互作用、抑制细胞因子的产生等机制来治疗SLE。相比于传统药物,靶向性生物制剂能够高特异性结合靶点,减少全身性副作用发生,提高治疗窗口从而提升疗效和安全性。
然而生物制剂并不能治愈SLE,也无法替代传统药物,主要作用仍是缓解病情,减少常规药物的用量。以泰它西普为例,其获批的适应症是“本品与常规治疗联合,适用于在常规治疗基础上仍具有高疾病活动的活动性、自身抗体阳性的系统性红斑狼疮成年患者。”
现实情况是,系统性红斑狼疮仍然存在着极大未满足的临床需求。
三、中国药企围攻SLE
SLE不仅是医学界的热门议题,同时也是各大药企的布局方向。截至2023年12月13日,全球共有353条在研管线用于治疗SLE。尽管关注度高,但SLE研发之路却极为凶险,有三分之一的在研管线都已处于终止状态,其中就包括辉瑞、安进、吉利德、罗氏等国际巨头。
图:SLE失败案例一览,来源:西部证券
国内企业布局SLE领域较晚,但进步明显,如荣昌生物的泰它西普就成功上市,填补了自主空白。目前在全球353条在研管线中,中国占了160条,涵盖JAKs、BTK、IFNI、BlyS、CD38和CD40等热门靶点。
具体来看,JAK抑制剂通过阻断JAK /STAT通路以阻断I型干扰素的作用,但目前尚未有JAK抑制剂获批用于治疗SLE,艾伯维的乌帕替尼目前处于临床III期,国内泽璟制药的杰克替尼、恒瑞医药的艾玛昔替尼等正在开展临床研究。
BTK抑制剂同样具有治疗SLE的潜力,国内的诺诚健华、百济神州均已开展针对SLE的临床试验研究。其中诺诚健华的奥布替尼治疗SLE的临床试验已到IIb期,有望成为最先攻克SLE的BTK抑制剂。
IFN受体拮抗剂通过抑制IFN-I高表达,来降低SLE患者疾病的严重程度,阿斯利康的阿尼鲁单抗目前正在中国开展SLE临床III期试验。国内智翔金泰的GR1603、荃信生物的QX006N等研发进度也较快。
BLyS、CD38、CD40等靶点在机制上展现出不俗的潜力,国内康诺亚的CM313、康缘药业的KYS202002A等已进入临床阶段。
除上述创新靶点外,发展不顺的CAR-T疗法有望在SLE领域焕发新春。CAR-T能够通过表达CD19 CAR特异性杀伤B细胞,或通过表达BCMA CAR特异性杀伤B细胞分化而来的浆细胞,从而有望达到深度清除SLE致病性B细胞的效果,触发免疫“重置”,甚至有望完全缓解SLE。
此外,国内屠呦呦团队研发的治疗疟疾药物双氢青蒿素也被认为对治疗SLE有效,目前由昆药集团正在开展临床二期试验。
回首数千年医学发展史,就是一部人类与疾病英勇斗争的进步史,一项疾病从束手无策到彻底征服,需要数代医学家的努力。在SLE这一困扰人类千年的疾病身上,我们正一步步揭开它的神秘面纱,而这一次中国药企所扮演的角色或将愈发重要。
本文来自微信公众号:医曜(ID:yiyao-jinduan006),作者:青栎