2024月24日,Nature正刊发表了来自拜耳子公司VividionTherapeutics的关于WRN抑制剂研发的文章,Vividion Therapeutics是一家专注使用化学蛋白质组学平台来面向不可成药靶点开发共价小分子抑制剂的biotech。
这篇文章报道了Vividion所开发的针对WRN解旋酶(WRN helicase)的共价变构抑制剂VVD-133214的化学蛋白质组学发现过程。
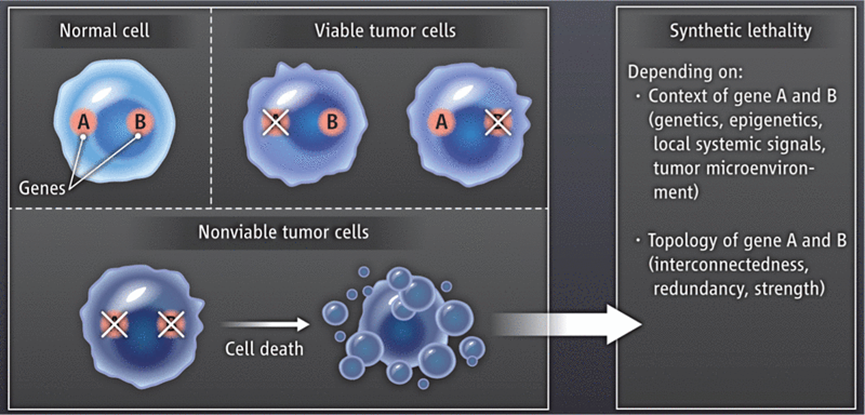
Werner综合征RecQ解旋酶(WRN)是近年来发现的“合成致死”新靶点,对微卫星不稳定性(MSI)肿瘤具有“合成致死”作用,是治疗MSI中立的潜力靶点。目前,尚无直接针对人类DNA或RNA解旋酶的上市药物,主要是因为开发选择性抑制这类蛋白的化合物具有较强的挑战性。
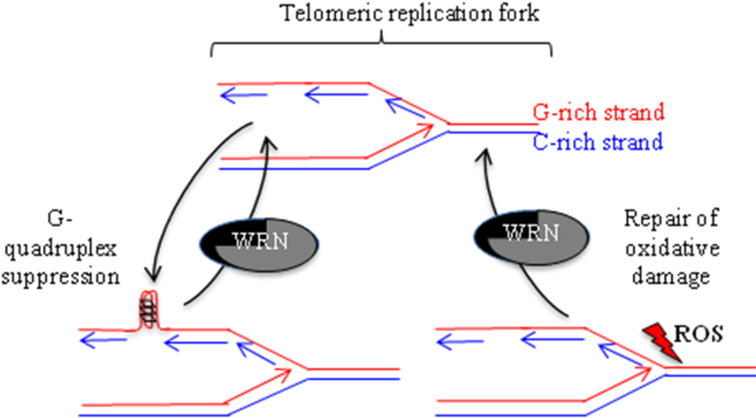
图1,WRN 解旋在DNA复制中的作用
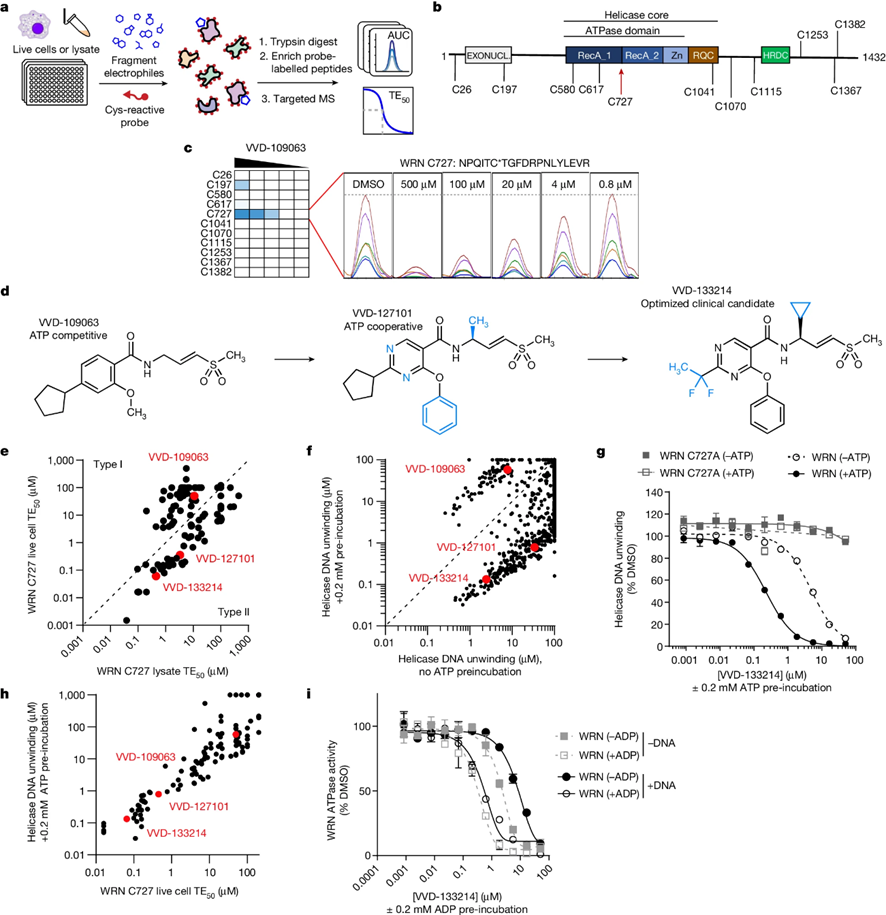
Vividion的研究人员开发了一种基于靶标的质谱化学蛋白质组学方法,用于量化小分子与细胞内或细胞裂解液中半胱氨酸残基共价结合的能力。
利用这一平台,研究人员筛选了一个包含数千个亲电小分子的化合物库,针对300多种在癌症和/或免疫疾病中起关键作用的蛋白质上的半胱氨酸残基。
研究发现了以VVD-133214为代表的一系列共价抑制剂,能够选择性地与WRN上的C727位点结合,具有低微摩尔范围WRN解旋酶抑制活性。
进一步的研究表明,VVD-133214与WRN蛋白的结合是核苷酸协同的,并且稳定了WRN的紧凑构象,导致MSI-H细胞中广泛的双链DNA断裂、核肿胀和细胞死亡,但在微卫星稳定的细胞中则不会。
图2,VVD-109063的筛选
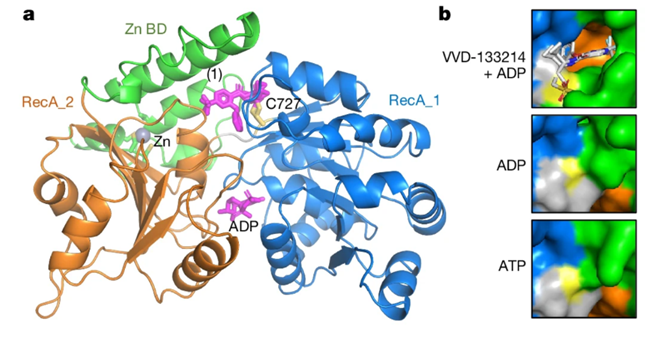
文章还披露了VVD-133214的发现过程及与WRN的共晶结构,共晶结构显示,VVD-133214 结合在WRN蛋白的ATPase RecA_1 和 RecA_2 结构域之间界面的疏水口袋内,并在C727 残基的硫原子和VVD-133214乙烯基砜的 β-碳之间观察到清晰的电子密度,证明了二者的共价连接。
VVD-133214与WRN的结合使其发生重大结构重排,导致RecA_2结构域(T705)、RecA_1结构域(E846和Y849)、Walker A基序(Y575)和铰链区(T728)之间形成一系列氢键稳定的闭合构象,从而抑制了WRN的解旋酶活性。
图3,VVD-133214与WRN解旋酶的共晶结构(PDB: 7GQU)
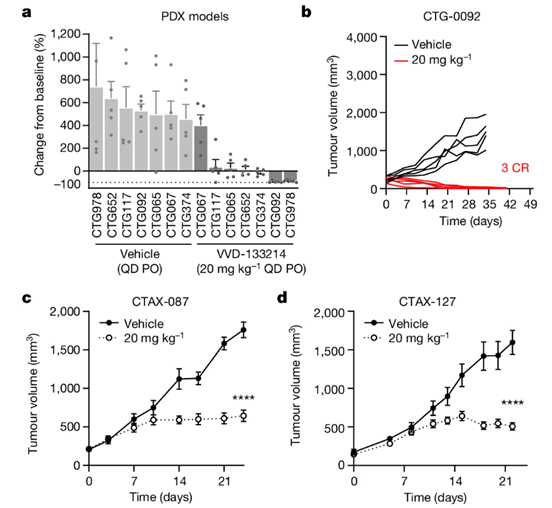
进一步的,研究人员在七个不同的MSI-H结直肠癌症患者衍生异种移植(PDX)模型中测试了VVD-133214的抗肿瘤活性。
每日20 mg/kg的口服剂量成功地减少了六个PDX模型中的肿瘤负担。此外,VVD-133214在两种不同的PDX模型中也显示出了不错的抗肿瘤疗效,这些模型来自同一位患者不同治疗阶段的样本:(1)手术后和FOLFOX治疗后(CTAX-087),以及(2)后来,随着免疫治疗耐药性的发展(CTAX-127)。
图4,VVD-133214 抑制 MSI-H PDX 模型中的肿瘤生长
这篇文章向我们展示了化学蛋白质组学在发现和优化针有挑战性的难成药靶点抑制剂的实用性,通过使用标记的共价探针,该方法可以同时评估化合物对数百种天然状态蛋白质的效力和选择性,尤其是在像WRN这样具有挑战性的靶点上应用,能够大大提高临床前的开发效率。
此外,VVD-133214的发现及其在MSI-H肿瘤中展现的治疗潜力也为那些对标准治疗和免疫疗法耐药的患者提供了新的治疗选择,VVD-133214与WRN蛋白共晶结构的披露则为WRN抑制剂开发的后来者提供了结构和功能上的见解,有望加速这一靶点药物的开发。
目前VVD-133214已完成IND-enabling研究,正在与罗氏合作在患有微卫星不稳定性癌症的患者中进行I期临床试验(NCT06004245)。
作者:LYQ