▉ 前言
免疫治疗已成为癌症治疗中不可或缺的一部分。整合素相关蛋白(CD47)作为一个关键的吞噬检查点,在与巨噬细胞上的信号调节蛋白α(SIRPα)相互作用时,作为“别吃我”的信号来保护细胞不被吞噬,引起了人们广泛关注。许多针对CD47/SIRPα的抗体在临床试验中显示出令人鼓舞的效果。同时,干扰CD47/SIRPα相互作用或调节CD47表达的小分子抑制剂的研究也在如火如荼地进行。本文综述了小分子抑制剂在转录、翻译和翻译后修饰水平上阻断CD47/SIRPα结合和调节CD47的研究进展,提供了针对CD47/SIRPα吞噬检查点的前景和策略。
https://www.crownbio.cn/blog/targeting-the-cd47-sirpa-axis-in-cancer-immunotherapy/
1.CD47的作用机制
针对适应性免疫系统的免疫检查点,如细胞毒性T淋巴细胞相关蛋白(CTLA)-4、程序性死亡(PD)-1及其配体PD-L1,已经在晚期癌症患者中取得了突破性的成功。然而,较低的客观应答率(15-30%)和耐药性的出现仍然是这些免疫检查点抗体的挑战。以先天免疫系统中的免疫检查点为目标可能提供一种新的解决方案。肿瘤相关巨噬细胞(TAMs)聚集在肿瘤组织周围,以及白细胞介素(IL)-10、转化生长因子(TGF)-β和其他细胞因子的分泌,形成免疫抑制的肿瘤微环境(TME),阻止CD8+T细胞向肿瘤组织的浸润。这些数据表明,靶向TAMs可以解锁免疫抑制的TME并刺激吞噬功能。
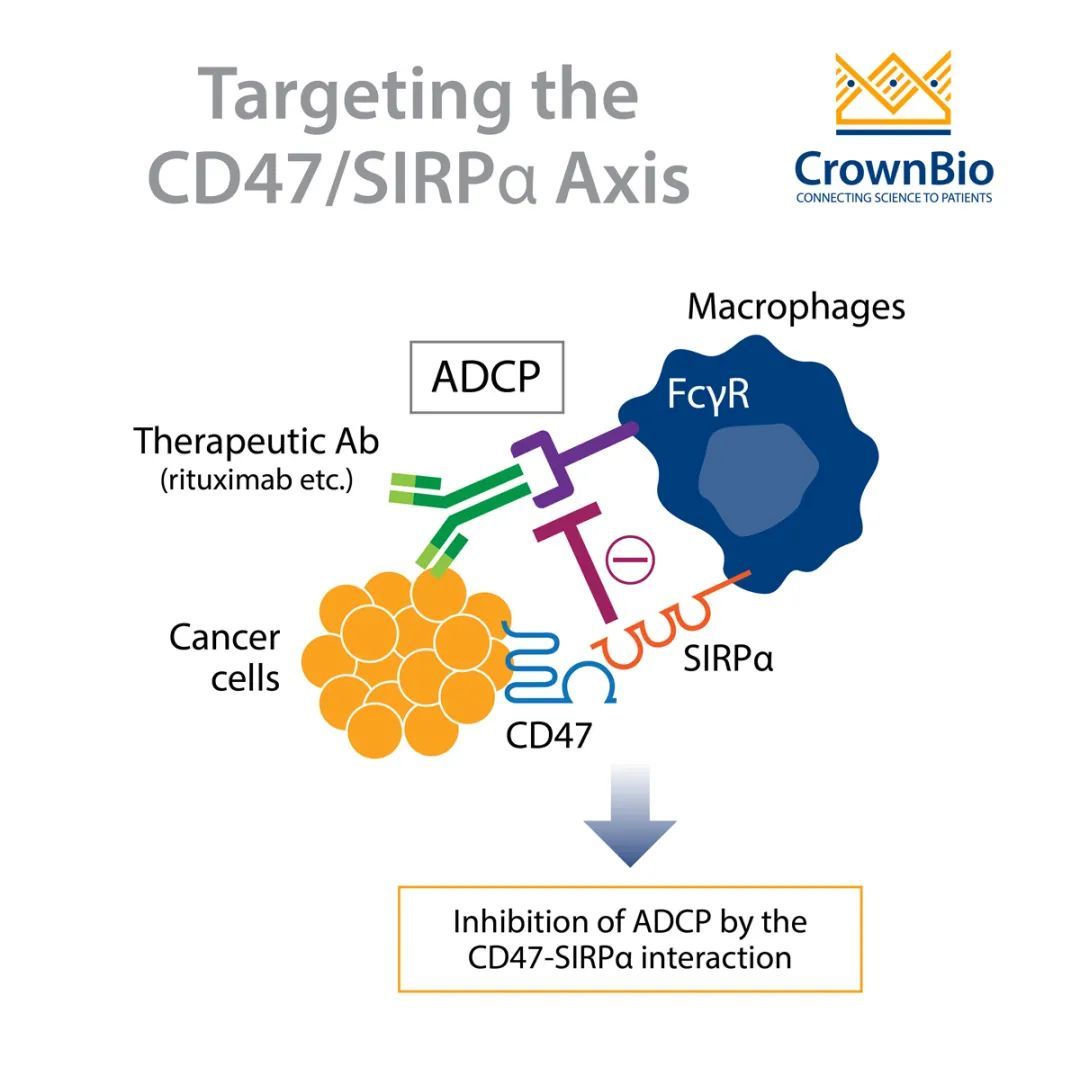
到目前为止,CD47是调节巨噬细胞吞噬功能的最有前景的靶点之一。从结构上看,五重跨膜蛋白CD47与短胞浆内C-末端尾巴相比,含有更大的胞外N-末端结构域。CD47上的细胞外IGV样结构域可以与位于髓系细胞(包括巨噬细胞)上的SIRPα结合,从而启动SIRPα胞内结构域中免疫受体酪氨酸抑制基序(ITIMs)的两个酪氨酸残基的磷酸化(图1)。
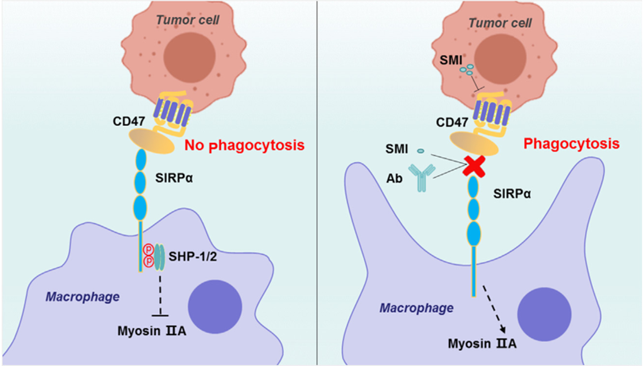
图1 肿瘤细胞和巨噬细胞之间CD47/SIRPα的作用机制。
当位于肿瘤细胞表面的CD47与巨噬细胞表面的SIRPα相互作用时,它将SIRPα的胞内部分磷酸化,然后激活SHP-1和SHP2,从而抑制肌球蛋白IIA,阻止巨噬细胞吞噬。当使用抗体(Ab)或小分子抑制剂(SMI)阻断或干扰CD47/SIRPα时,CD47/SIRPα被破坏会导致巨噬细胞吞噬功能的激活。
ITIMs的磷酸化重新募集并激活磷酸酶SHP1/2,导致该级联中的下游蛋白--非肌肉肌球蛋白IIA受到抑制,最终抑制吞噬作用。CD47在不同细胞类型中的表达水平不同。它在红细胞上的高表达显示了它的保护功能。此外,它的表达对控制循环中造血干细胞的命运至关重要。更重要的是,CD47通常在多种癌细胞中过表达,以帮助它们逃避免疫监视。阻断CD47/SIRPα的结合导致SHP1/2的募集和激活失败,从而促进吞噬功能。在这个过程中,抗原提呈细胞(APC)的交叉激发也被启动,导致适应性免疫系统的激活。体外和体内研究表明,CD47/SIRPα阻断抗体显著增强巨噬细胞吞噬、树突状细胞(DC)交叉呈递和中性粒细胞介导的对癌细胞的杀伤。
抗CD47单克隆抗体(靶向CD47)、SIRPα融合蛋白(靶向CD47)、抗SIRPα抗体(靶向SIRPα)和双特异性抗体(双靶点)在治疗上已成功阻断CD47/SIRPα吞噬检查点。这些抗体正被用于治疗各种癌症,包括急性髓系白血病(AML)、非霍奇金淋巴瘤(NHL)、膀胱癌、乳腺癌、胃癌和肺癌。最近,抗CD47单克隆抗体Magrolimab(Hu5F9-G4)联合阿扎西丁治疗骨髓增生异常综合征(MDS)的Ⅲ期临床试验启动(NCT04313881)。另一种抗CD47的单克隆抗体TJC4(TJ011133)正在进行治疗AML的II期临床研究(NCT04202003)。这些抗体的临床研究表明,CD47/SIRPα是一个不同于适应性免疫检查点的有希望的靶点。
2.CD47小分子抑制剂的研究进展
尽管针对CD47的一些抗体已经显示出可接受的治疗效果,但诸如贫血等不良反应是不可避免的。这是因为CD47是一种普遍表达的细胞表面蛋白,在红细胞上也有表达。此外,由于抗体在人体内的半衰期较长,从而延长了不良反应。相比之下,小分子化合物由于其较短的代谢半衰期和灵活的体内药物暴露,在某些方面具有可控的副作用。此外,小分子抑制剂由于分子量小,更容易进入肿瘤细胞。已报道的针对CD47轴的小分子抑制剂包括在转录、翻译和翻译后修饰水平上破坏CD47/SIRPΑ相互作用的阻断剂和CD47的调节剂(图2)。
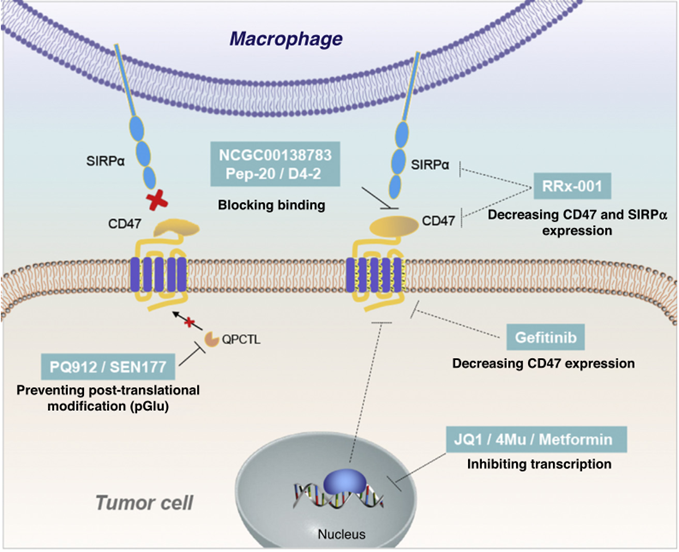
图2 针对分化簇47/信号调节蛋白α(CD47/SIRPα)轴的小分子抑制剂。
PEP-20、D4-2和NCGC00138783阻断CD47和SIRPα的结合;PQ912和SNE177阻止CD47翻译后修饰(焦谷氨酸形成),从而干扰CD47和SIRPα的结合;二甲双胍、JQ1和4Mu在转录水平降低CD47的表达;RRx-001同时降低CD47和SIRPα的表达;吉非替尼降低CD47的表达。二甲双胍、JQ1、4Mu、RRx-001和吉非替尼的详细调控机制尚不清楚。
2.1. 直接阻断CD47与SIRPα结合的小分子抑制剂
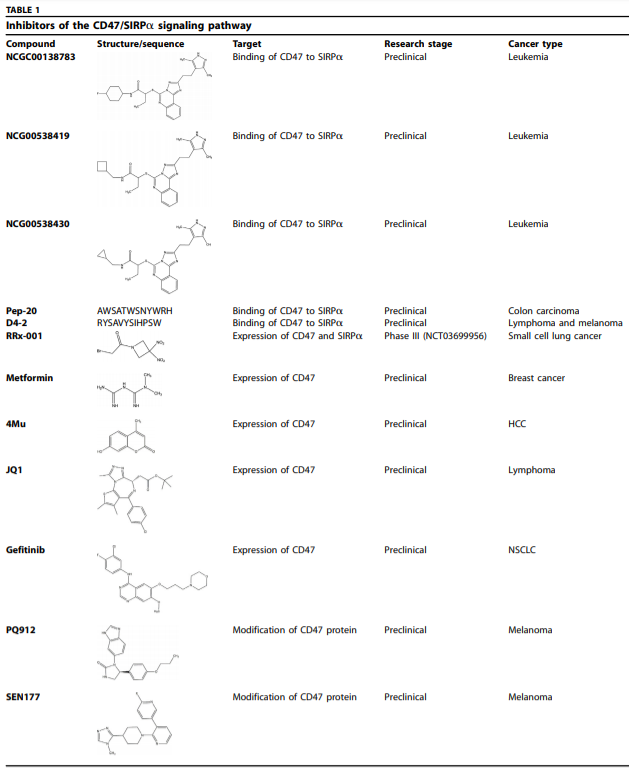
NCGC00138783、PEP-20和D4-2是已报道的三种直接阻断CD47和SIRPα相互作用的抑制剂。它们的结构和序列如表1所示。NCGC00138783和PEP-20都被报道与CD47结合以发挥其封闭功能;D4-2通过与SIRPΑ结合来干扰CD47/SIRPα的相互作用。
表1 CD47/SIRPα信号通路的抑制剂
2.1.1 NCGC00138783
使用定量高通量筛选(HTS),Miller等人发现NCG00138783对CD47/SIRPα干扰有很强的抑制作用。对NCGC00138419和NCGC00138430的理化性质和药效性的进一步优化导致了NCGC00138419和NCGC00138430的发现(表1)。在生化和基于细胞的分析中,这三个类似物都抑制CD47/SIRPα结合。NCG00138783以浓度依赖的方式抑制CD47与SIRPα的结合,IC50为~50 μM。这些化合物似乎选择性地与CD47/SIRPα结合位点相互作用,这可以减少由于阻断CD47与SIRPα以外的蛋白质的相互作用而引起的一些相关的不良影响。
2.1.2 Pep-20
据报道,被设计为CD47抑制剂的Pep-20肽可以阻断人和小鼠CD47/SIRPα的相互作用,其IC50分别为24.56和12.03 μM。经过D-氨基酸修饰的衍生物Pep20-D12在体内半衰期延长,与CD47的结合能力相似。巨噬细胞对MCF7、H729和Jurkat细胞的吞噬作用强于抗CD47抗体(B6H12)。在治疗方面,2 mg/kg的PEP-20可抑制CT26和MC38荷瘤小鼠的肿瘤生长,延长其总体生存期。体内研究还表明,PEP-20-D12联合放射治疗后,肿瘤体积缩小。此外,PEP-20连续14天对C57BL/6小鼠的血液毒性最小。
2.1.3 D4-2
最近,一种中等大小的大环肽D4-2被设计为SIRPα阻滞剂,其IC50为0.18 μM,可阻断小鼠CD47和SIRPΑ的结合;它还显示出在Raji,BT474和NCI-N87细胞中的吞噬功能增加,并以剂量依赖的方式联合利妥昔单抗或曲妥珠单抗。在非肥胖糖尿病SCIDγ(NSG)小鼠模型中也观察到了优化效应。毒性研究表明,免疫功能正常的小鼠每天服用D4-2,连续6天,并不会导致红细胞水平下降。
2.2 在转录和翻译水平上抑制CD47表达的小分子抑制剂
RRx-001、二甲双胍、4-甲基伞形酮(4-Mu)、JQ1和吉非替尼已被报道在转录和翻译水平上抑制CD47的表达。其中,RRx-001已进入III期临床试验。
2.2.1 RRx-001
小分子化合物RRx-001(1-溴乙酰基-3,3-二硝基氮杂环丁烷),来自航空航天工业,作为癌症疗法正处于III期临床试验。结果显示,2 μM RRx-001在体外将巨噬细胞极化从M2表型转变为M1表型,并显著下调CD47的表达。在RRx-001单独治疗期间,体内巨噬细胞的缺失显示出抗肿瘤作用的减弱。其代谢产物RRx-001-Cys-Ox也降低了CD47的表达,从而增强了RRx001的抗肿瘤作用。用RRx-001治疗荷B16黑色素瘤的小鼠,结果显示M1表型巨噬细胞占优势。从机制上讲,RRx-001通过抑制CD47的正调控因子c-MYC来抑制肿瘤细胞中CD47的表达。
RRx-001的临床研究显示了令人鼓舞的结果。来自NCT02489903的结果显示,RRx-001治疗的有效率为30%。此外,阳性反应似乎与肿瘤组织中的高巨噬细胞浸润相关。在一项剂量递增研究(NCT01359982)中,RRx-001在剂量高达83 mg/m2时没有引起剂量限制性毒性。值得注意的是,与抗CD47抗体不同,RRx-001没有表现出任何血液毒性;最常见的不良反应是注射部位的短暂性疼痛。
2.2.2 Metformin
二甲双胍是一种口服降糖药物,已使用数十年,具有良好的临床安全性和耐受性。最近,人们发现它能显著抑制肿瘤的发展,部分是通过免疫刺激调节。二甲双胍治疗抑制了M2极化巨噬细胞的比例,并导致M2巨噬细胞向M1巨噬细胞的转变。研究进一步证实二甲双胍在体外是一种CD47抑制因子。10 mM二甲双胍处理乳腺癌细胞后,CD47在mRNA水平下调50%。然而,二甲双胍调控CD47的确切机制仍不清楚。
2.2.3 4-Methylumbelliferone
4Mu是透明质酸合成的抑制剂。在体外,4Mu可增加腹腔巨噬细胞对肝细胞癌(HCC)细胞的吞噬作用。在原位肝癌小鼠模型中,4Mu与编码IL-12的腺病毒(ADIL-12)联合使用可显著缩小肿瘤体积并显著提高总存活率。0.5 mM的4Mu预处理72h后,HEPA 129细胞表面CD47在mRNA和蛋白水平的表达均降低。此外,在肝癌小鼠模型中,4Mu治疗导致CD47mRNA水平下降50%。然而,4Mu对CD47的调控机制还有待进一步验证。
2.2.4. JQ1
JQ1是一种溴域和端外(BET)蛋白的小分子抑制剂。BET家族蛋白是介导组蛋白乙酰化的关键“读者”,因此是癌基因蛋白的重要调节因子,如原癌基因(c-MYC)。JQ1降低了CD47和PD-L1在急性淋巴细胞白血病、黑色素瘤和非小细胞肺癌(NSCLC)细胞上的表达。特别是,10 μM的JQ1使c-MYC的表达失活,并使CD47在转录和翻译水平上的表达均降低了50%以上。Li等人也得到了类似的结果。在弥漫性大B细胞淋巴瘤中。两项研究都证实JQ1通过c-MYC介导的途径下调CD47的表达。、
2.2.5. Gefitinib
吉非替尼是第一代竞争性酪氨酸激酶表皮生长因子受体抑制剂(EGFR-TKIs),用于治疗非小细胞肺癌。它可逆地与EGFR ATP结合域结合,抑制细胞内磷酸化和下游信号通路。EGFR-TKI,包括第一代和第二代抑制剂,调节TME中免疫检查点PD-L1的表达和肿瘤突变负荷。最近,人们注意到,单独使用吉非替尼可以显著下调非小细胞肺癌细胞(如PC9、H1437和H1573)中CD47的表达,并增加DC的吞噬功能。50 nM的吉非替尼作用于PC9细胞48h后,CD47蛋白水平明显降低(降低40%)。与单用相比,联合应用CD47抗体可增强巨噬细胞的吞噬功能。
2.3. 针对CD47/SIRPΑ的小分子抑制剂
在翻译后修饰水平上是指蛋白质生物合成后的酶调节,使蛋白质成熟并使其能够执行功能。到目前为止,调节CD47焦谷氨酸形成的谷氨酰肽环转移样蛋白(QPCTL)抑制剂,如SEN177和PQ912,已经被报道对CD47-SIRPα相互作用的影响。
2.3.1 QPCTL抑制剂
最近,QPCTL(称为isoQC)被发现是CD47/SIRPα的重要调节因子。Logtenberg等人。进一步确认QPCTL是CD47吞噬检查点的重要酶调节因子,在CD47/SIRPα相互作用中起着不可或缺的作用。QPCTL调控CD47焦谷氨酸(PGlu)的形成,从而干扰其与SIRPα的相互作用。用SEN177和PQ912抑制QPCTL导致CD47“改变”,对抗CD47抗体或人SIRPα融合蛋白几乎没有亲和力。SEN177在体外可抑制QPCTL的功能,增强抗CD20抗体的抗体依赖性细胞吞噬功能和细胞毒作用。此外,本研究还证实QPCTL抑制剂联合抗CD47抗体可增强抗肿瘤作用。QPCTL治疗后,体内中性粒细胞介导的对癌细胞的杀伤率也显著增加。
3.CD47小分子抑制剂相关的挑战和策略
CD47小分子抑制剂领域尚未成熟,但前景看好。调节CD47的小分子抑制剂在癌症和其他疾病中的确切作用机制尚不清楚。之前讨论的许多小分子抑制剂缺乏体内和临床数据。因此,这里我们重点介绍了可以用来应对小分子抑制剂开发挑战的策略。
3.1. 靶向CD47/SIRPα的结合
与CD47抗体相比,小分子具有更小的体积和更小的结合表位,这不会阻止CD47与其他成员(如血小板反应蛋白家族的成员)结合,从而维持CD47的其他功能。然而,小分子的亲和力和选择性很难达到抗体的水平,这意味着小分子的脱靶效应很严重。蛋白质-蛋白质相互作用的结合力更多地依赖于极性接触,而小分子具有更多的杂原子和分子-蛋白质相互作用,更多地依赖芳香族接触;因此,小分子抑制剂的结合能力弱于抗体。为了增加这种亲和力,分子量变得更大,这会导致亲脂性增加,在水中溶解性差,口服吸收困难。
要解决这些问题,关键是要利用CD47/SIRPα共晶结构来确定关键结合位点。最短的多肽药效团可以结合到小分子支架上,对CD47/SIRPα发挥抑制作用。小分子抑制剂Aur-104是基于肽/模拟肽筛选的,在体内表现出良好的抗肿瘤作用和降低免疫原性。
另一方面,相当多的化合物具有固有的荧光性质,特别是带有羟基蒽醌荧光基团的化合物。为了提高荧光小分子化合物的稳定性,降低假阳性率,需要一套互补的初筛和反筛选方法。具体地说,时间分辨福斯特共振能量转移 (TR-FRET) 分析用于初步筛查,它应用低能量激发并引起高能量排放。放大发光接近均相分析(AlphaScreen)采用高能激发并产生低能量发射,是正交验证性试验的理想选择。
功能分析(包括CD47/SIRPα结合,体外和体内吞噬作用),被用于候选化合物的药理学评价,是开发针对CD47的小分子抑制剂的另一个重要部分,这与物种特异性有关。人的SIRPα对人和猪的红细胞有很强的亲和力,但对小鼠、大鼠或牛的亲和力较低。相反,在小鼠巨噬细胞J774A.1上表达的SIRPα表现出与人和小鼠CD47相似的亲和力,由吞噬速率证实。然而,小鼠的SIRPΑ与人CD47的结合似乎各不相同。在BALB/c和C57BL/6小鼠中,非肥胖糖尿病小鼠的巨噬细胞与人CD47的结合效率高于与巨噬细胞的结合。因此,非肥胖型糖尿病品系小鼠可能是评价受这些化合物调控的巨噬细胞体内吞噬功能的较好模型。巨噬细胞缺失模型也是进一步评估CD47功能所必需的。
3.2. CD47在转录和翻译水平的靶向表达
考虑到开发破坏CD47/SIRPα相互作用的小分子抑制剂的困难,探索调节CD47表达的抑制剂是另一种可能的途径。已报道的CD47调节因子包括TME中的癌基因和细胞因子,其中大部分通过转录因子发挥作用。最近,c-MYC和核因子(NF)-kB被认为是调控CD47表达的关键转录因子。缺氧诱导因子-1a(HIF-1a)也被证明可以抑制CD47的转录。值得注意的是,报道显示了一种细胞上下文依赖的机制,这可能会对这一策略构成挑战。
此外,CD47/SIRPα抑制后,广泛分布的巨噬细胞可能吞噬包括红细胞在内的正常细胞。以往的临床研究表明,抗CD47抗体引起的贫血是不可忽视的。小分子RRx-001和PEP-20提供了克服这种贫血的潜力,但其他小分子抑制剂是否会影响体内的红细胞还需要进一步的研究。在这种情况下,在针对CD47的小分子抑制剂的开发中,血液毒性仍然是化合物安全性评估的一个指标。
抗体-抗体联合治疗的重大进展为小分子CD47抑制剂与其他抗体的联合治疗提供了框架。单用一些针对CD47/SIRPα的小分子,如D4-2,吞噬功能的增加是有限的,但这些小分子与其他抗体的联合策略显著增强了它们的抗肿瘤效果。D4-2联合利妥昔单抗比单独使用利妥昔单抗更明显地抑制肿瘤生长。此外,在一项旨在加强小分子抑制剂和抗体联合治疗可行性的I期临床试验(NCT02518958)中,RRx-001和nivolumab联合治疗晚期恶性肿瘤显示出良好的活性,疾病控制率为67%。
3.3. 针对CD47/SIPRα的翻译后修饰水平(PTMS)
作为一种跨膜蛋白,CD47出现在细胞表面的形态结构决定了其与SIRPα的结合亲和力。这为通过干扰PTMS来调节CD47/SIRPα的功能提供了理论基础,从而可以克服直接阻断CD47/SIRPα的一些缺陷。抗原沉默通常被认为是抗体靶向内化膜抗原的一个挑战,而内化膜抗原在正常细胞上过度表达。这在抗CD47治疗中仍然是一个问题。然而,QPCTL是一种酶,针对它的抑制剂可以绕过这个问题。同时,新到达细胞表面的CD47缺乏pGlu的形成,并且不能在小分子抑制QPCTL的情况下与SIRPα结合。此外,QPCTL抑制剂仅对红细胞表面的pGlu-CD47影响最小,因为这些细胞缺乏细胞核和蛋白质合成,导致较低的血液毒性。QPCTL基因敲除小鼠的安全性进一步得到证实,这些小鼠仍然健康。
CD47/SIRPα的糖基化和泛素化也值得考虑。Parthasarathy等人,在酵母模型中发现糖基化是锚定在细胞膜上的CD47所必需的。然而,另一项研究报道了不同的结果,表明CD47的糖基化不影响对中国仓鼠卵巢(CHO)细胞膜的输出。到目前为止,几乎没有关于CD47泛素化的研究,但是预测CD47E3连接酶的生物信息学分析显示,有5个E3连接酶具有中等置信水平。这将使基于PROTAC技术的小分子抑制剂得以开发。2004年,日本的一个研究小组发现SIRPα是名为SCFNFB42的E3泛素连接酶的底物,为SIRPα泛素化提供了灵感。这些数据表明有可能开发小分子抑制剂来对抗SIRPα的糖基化和CD47/SIRPα的泛素化。
▉ 结论
虽然针对CD47免疫检查点的抗体,如Magrolimab,已经显示出良好的抗肿瘤效果,一些已经进入III期临床试验,但开发小分子抑制剂也同样重要,因为它们比抗体具有优势。首先,小分子抑制剂不是免疫原性的,与抗体相比半衰期更短,这使得它们的副作用是可控的。其次,一些CD47抗体可以引起凝集,因为抗体与高密度红细胞膜决定簇结合,如血糖素A,这可以通过小分子抑制剂来避免。此外,小分子抑制剂具有口服给药的潜力,可以改善患者的依从性。除了关注CD47,靶向SIRPα的小分子抑制剂也是可行的。与抗体相比,小分子抑制剂将更容易渗透到细胞内,并抑制下游信号通路,阻止下游信号激活以重新刺激吞噬作用。
总体而言,以CD47/SIRPα为靶点启动先天免疫以抑制肿瘤进展是一个很有前途的策略。我们希望这一综述将进一步激励科学家开展针对CD47/SIRPα吞噬检查点的小分子抑制剂的研究。
参考文献: Yu WB, Ye ZH, Chen X, Shi JJ*,Lu JJ*. The development of small-molecule inhibitorstargeting CD47. Drug Discov Today. 2021, 26(2): 561-568.