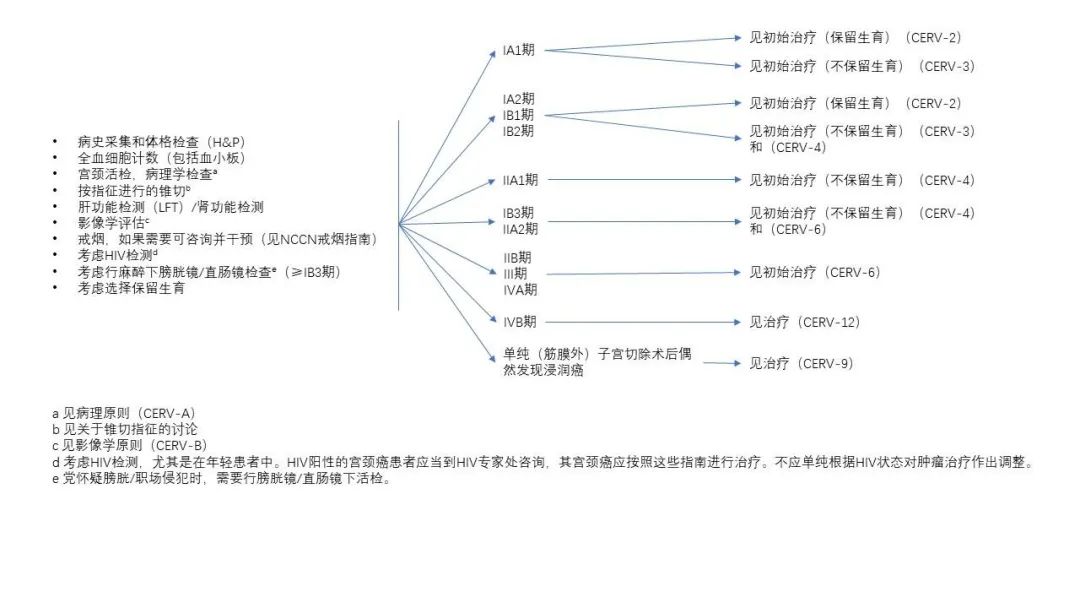
初始工作流程
I期
不保留生育
考虑通过放射平片(X线平片)行胸部影像学检查。如果观察到异常,则可行胸部CT平扫。
考虑盆腔增强MRI以评估局部病灶范围(推荐用于FIGO IB2-IB3期)。
FIGO IB1期以上行全身PET/CT(推荐)或胸/腹/盆CT或PET/MRI。
对于行全子宫切除术(TH)意外发现宫颈癌的患者,考虑全身PET/CT或胸/腹/盆CT以评估转移病灶;行盆腔MRI以评估盆腔残留病灶。
保留生育
考虑放射平片(X线平片)行胸部影像学检查。如果观察到异常,则可行胸部CT平扫。
行盆腔MRI(推荐)以评估局部病灶范围及肿瘤据宫颈内口的距离,如果有MRI禁忌时行经阴道盆腔超声。
对于FIGO IB1-IB2期,行全身PET/CT(推荐)或胸/腹/盆CT。
其他初始影像学检查需基于症状学和临床上对转移病灶可能性的考虑b。
II-IVA期
行全身PET/CT(推荐)或胸/腹/盆CT以评估转移病灶。
考虑盆腔增强MRI以评估局部病灶范围。
其他初始影像学检查需基于症状学和临床上对转移病灶可能性的考虑c。
对于行全子宫切除术(TH)意外发现宫颈癌的患者,考虑全身PET/CT或胸/腹/盆CT以评估转移病灶;行盆腔MRI以评估盆腔残留病灶。
随访+影像学检查推荐
I期
不保留生育
影像学检查需基于症状学和临床上对转移病灶可能性的考虑b。
FIGO IB3期的患者或因为存在高危因素d需要术后辅助放疗或放化疗的患者,可在完成治疗后3-6个月后行全身PET/CT。
保留生育
考虑在术后6个月,随后的2-3年中每年一次行盆腔增强MRI。
其他影像学检查需基于症状学和临床上对复发/转移病灶可能性的考虑b。
II-IV期
完成治疗后3-6个月内行全身PET/CT(推荐)或胸/腹/盆增强CT。
考虑在完成治疗后3-6个月行盆腔增强MRI。
其他影像学检查需基于症状学和临床上对复发/转移病灶可能性的考虑e。
IVB期或复发
适当的影像学检查(CT,MRI,或PET/CT)以评估对治疗的反应性,并决定后续治疗。
怀疑复发或转移
全身PET/CT。
考虑盆腔MRI。
a 本指南中MRI和CT均为增强,除非有禁忌症。胸部CT筛查不需要增强。
b 这些因素可能包括查体中的异常发现或盆腔,腹部,或肺部症状。
c 这些因素可能包括查体中的异常发现,肿瘤体积大(>4cm),发现或治疗上的延迟,以及盆腹腔或肺部症状。
d 危险因素可能包括淋巴结阳性,宫旁阳性,切缘阳性,或局部宫颈因素(见Sedlis标准 CERV-E)。
e 这些因素可能包括腹部查体中的异常发现,如可触及的肿块或淋巴结,或新出现的盆腔,腹部,或肺部症状。
参考文献
1Salani R, Khanna N,Frimer M, et al. An update on post-treatment surveillance and diagnosis ofrecurrence in women with gynecologic malignancies: Society of GynecologicOncology (SGO) recommendations. Gynecol Oncol 2017;146:3-10.
2Atri M, Zhang Z,Dehdashti F, et al. Utility of PET-CT to evaluate retroperitoneal lymph nodemetastasis in advanced cervical cancer: Results of ACRIN6671/GOG0233 trial.Gynecol Oncol 2016;142:413-419.
3Rajendran JG, GreerBE. Expanding role of positron emission tomography in cancer of the uterinecervix. J Natl Compr Canc Netw 2006;4:463-469.
4Lakhman Y, Akin O,Park KJ, et al. Stage IB1 cervical cancer: role of preoperative MR imaging inselection of patients for fertility-sparing radical trachelectomy. Radiology2013;269:149-158.
5Elit L, Reade CJ.Recommendations for follow-up care for gynecologic cancer survivors. ObstetGynecol 2015;126:1207-1214.
6Sala E, Rockall AG,Freeman SJ, et al. The added role of MR imaging in treatment stratification ofpatients with gynecologic malignancies: what the radiologist needs to know.Radiology 2013;266:717-740.
7Balleyguier C, SalaE, Da Cunha T, et al. Staging of uterine cervical cancer with MRI: guidelinesof the European Society of Urogenital Radiology. Eur Radiol 2011;21:1102-1110.
8Sala E, Micco M,Burger IA, et al. Complementary prognostic value of pelvic MRI and whole-bodyFDG PET/CT in the pretreatment assessment of patients with cervical cancer. IntJ Gynecol Cancer 2015;25:1461-1467.
9Bhatla N, Berek JS,Fredes MC, et al. Revised FIGO Staging for carcinoma of the cervix uteri. Int JGynecol Obstet 2019;145:129-135 and Corrigendum to "Revised FIGO Stagingfor carcinoma of the cervix uteri” [Int J Gynecol Obstet 2019;145:129-135] IntJ Gynecol Obstet 2019;147:279-280.
影像学原则
第一页
初始工作流程
I期
不保留生育
- 亚条目修改:FIGO IB3IB1期以上行全身PET/CT(推荐)或胸/腹/盆CT或PET/MRI。
- 亚条目删除:在FIGO IB1-IB2期考虑全身PET/CT或胸/腹/盆CT。这一推荐被整合到另一个条目中。
保留生育
- 亚条目修改:对于FIGO IB1-IB2期,考虑行全身PET/CT(推荐)或胸/腹/盆CT。
修改的分期:II-IVA期
第二页
随访/监测:IVB期或复发中加入了推荐的影像学检查方式。
评估和手术分期原则
第一页
切除手术的类别以及宫颈癌治疗的合理性
修改了第四点:“标准的和经典的推荐的根治性子宫切除方法是开腹的方法(1类证据)。之前版本的指南中写到根治性子宫切除可通过开腹或微创方式进行,微创手术可使用传统腹腔镜或机器人技术。然而,当前几个关键的研究已经质疑了开腹手术与微创手术的等效性。一个前瞻性随机试验证实…”
删除的点:考虑到最近的一项对于早期宫颈癌女性的随机对照研究发现微创手术相比于开腹手术预后显著更差,应当向患者详细说明不同手术方式的短期和长期预后差异以及肿瘤学风险。
第三页
脚注c是新的:在III期随机FILM研究中,吲哚啨绿(ICG)被证实不劣于异硫蓝。(Frumovitz M, Plante M, Lee PSet al. Near-infrared fluorescence for detection of sentinel lymph nodes inwomen with cervical and uterine cancers (FILM): a randomised, phase 3, multicentre,non-inferiority trial. Lancet Oncol 2018;19:1394-1403)
第四页
脚注g是新的:没有标准的超分期方案。典型的超分期包括对大体淋巴结行连续切片,并行H&E染色,包括或不包括细胞角蛋白免疫组化染色,以进行评估。见病理学原则(CERV-A)。
第五页
表1:宫颈癌切除作为初始治疗
手术方式推荐修改如下:
对比子宫切除术类型
筋膜外子宫切除(A型):经阴道或开腹或微创
改良根治性子宫切除(B型):开腹或微创
根治性子宫切除(C1型):开腹或微创
对比保留生育的宫颈切除术类型
根治性宫颈切除:经阴道或开腹或微创(微创为2B类证据)
脚注m是新的:缺少关于微创手术行宫颈切除的肿瘤学结局数据。
放疗原则
第一页
总体原则:修改了第三点,近距离放疗是所有不适宜手术的初发宫颈癌患者的根治性治疗的关键组成部分。其方式为腔内±和/或间质内放疗。
第二页
治疗信息——体外放射线
第二点修改为:“IMRT可能有助于最小化肠道和…受到的照射剂量”
剂量方案——体外放射线
修改为:“覆盖显微镜下受累的淋巴结需要EBRT的剂量大约为40-45Gy(在传统的…)”
第三页
对于完整宫颈的根治性放疗
修改为:“…原发宫颈肿瘤随后使用近距离放疗照射,剂量为30-40Gy,使用影像学引导(推荐)或照射到A点(以低剂量率[LDR]等效剂量),使A点的总剂量(如指南中所推荐)对小肿瘤达到80Gy,对更大体积的肿瘤达到85Gy以上。对于每一个小肿瘤(无法手术的IA1或IA2期患者可考虑EQD2D90剂量70-80Gy)。大体受累的未切除淋巴结可以额外的10-15Gy高共形(低剂量)EBRT照射,当使用影像学对EBRT引导时必须小心,以除外或严格限制正常组织的照射剂量…”
子宫切除术后辅助放疗
修改为:“…按照最小范围,以下组着需被覆盖:阴道断端上3-4cm,宫旁,紧邻的淋巴结区(如髂外和髂内,闭孔,骶前淋巴结)。如已知有淋巴结转移,放射野上缘应当适当增加(如前面描述的)。一般推荐IMRT标准分割剂量为 40-50Gy…”
第五页
剂量方案——近距离放疗
第二点修改为:“…治疗目标应包括对高危CTV(HR-CTV)等效剂量2Gy(EQD2),D90为≥8080-85Gy;然而,对于大病灶或反应性差的患者,剂量目标应为HR-CTV D90≥87Gy…”
第三点修改为:“…使用高剂量率(HDR)近距离放疗的临床医生可通过线性二次型方程将HRD标称剂量转化为A点生物等效LDR剂量(http://www.americanbrachytherapy.org/guidelines/)。当与EBRT结合时,多个近距离放疗模式曾被使用过。然而,更常见的HDR方式之一是5个插入点,每个提供6Gy的标称剂量到A点。这一模式使得30Gy的标称HDR剂量被分为5部分…”
删除的点:鼓励将影像学引导的近距离放疗用于HR-CTV。最常见的经典近距离放疗剂量参数所使用的系统中包括了确定的A点剂量,同时整合了基于解剖学的针对子宫和阴道内“放射源负荷与活性分布”的特定指南。标准化B点,膀胱和直肠等点的剂量也要计算。目前的三维图像引导近距离放疗旨在最优化肿瘤区域的植入剂量,同时尽可能的减少临近膀胱,直肠,和肠管结构的剂量。然而,根据经验与肿瘤控制效果,大部分临床治疗是基于A点剂量系统。当尝试改进影像学引导的近距离放疗中所使用的剂量时,应当注意不能使肿瘤部位的剂量小于A点系统中推荐的剂量。
宫颈癌全身治疗方案
标题页中删除了“强烈考虑临床试验”。这一建议被列入指南脚注中。
放化疗
其他推荐方案:删除了顺铂/氟尿嘧啶这一选择。
复发或转移性疾病
一线组合方案
优选方案中删除了下列药物,其被放入其他推荐方案中:
- 顺铂/紫杉醇(1类证据)
- 卡铂/紫杉醇(对之前接受过顺铂治疗的患者为1类证据)
- 拓扑替康/紫杉醇/贝伐单抗(1类证据)
- 拓扑替康/紫杉醇
二线方案
NTRK基因融合阳性肿瘤使用拉罗替尼或恩曲替尼(2类证据)被列为一个选择。其属于“在特定情况下有效”这一类别。
脚注g是新的:见NCCN免疫治疗相关毒性管理指南