原发性耐药(primary resistance):指肿瘤患者初始接受免疫治疗完全无反应,相反,病情发展迅速或进展。
获得性耐药(acquired resistance):指肿瘤患者初始对免疫治疗较好的应答,但是随后出现进展。
尤其是目前国内已有多款PD-1/PD-L1免疫检查点抑制剂药物获批上市(详见:「不限癌种」MSI-H/dMMR实体瘤再迎PD-1新药!附国内已上市16大PD-1/PD-L1类免疫药物获批适应症汇总!)。越来越多的患者用上了这类免疫治疗药物。
相应地,用过PD-1/PD-L1免疫药物的患者基数变大,耐药问题显得格外突出且亟需解决,耐药后很多患者面临无有效药物可用的困境。
那么PD-1/PD-L1单抗耐药后,患者只能选择化疗吗?有哪些治疗方案可以让患者再次获益呢?
PD-1耐药后继续使用,仍有19%患者可获益
美国FDA进行了一项大规模的回顾性研究,汇总分析了包括Keynote-006和Checkmate-067等大型Ⅲ期临床试验在内的黑色素瘤临床数据,共筛选了2624位用过PD-1抑制剂治疗的患者,其中原发性耐药或获得性耐药的患者占比52%(1361/2624)。
接下来1361位耐药的患者经研究者评估有692例患者体能状态不错,决定继续用药,而剩下的669例患者则彻底放弃了PD-1抗体治疗。经过长期随访发现,
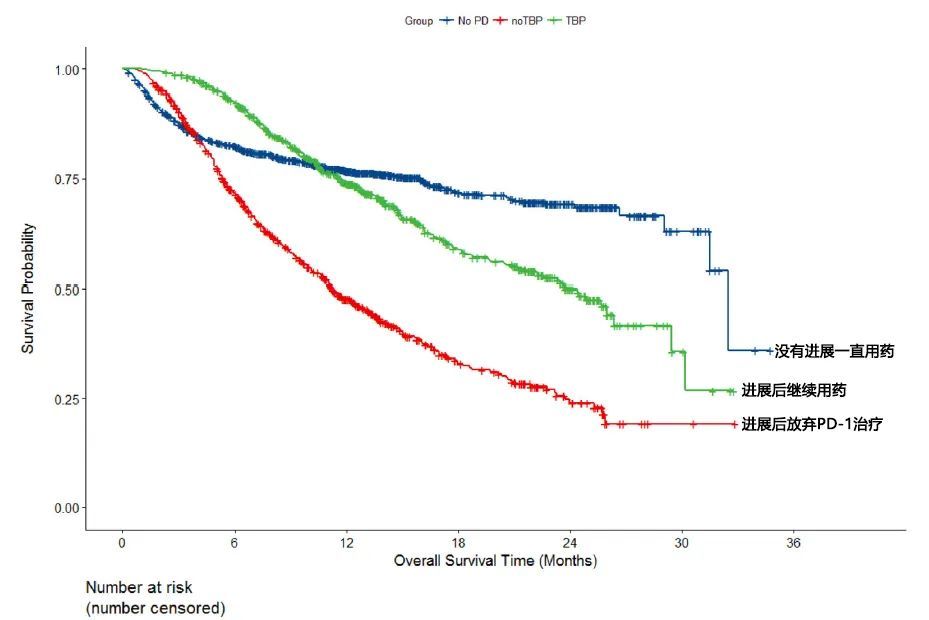
PD-1有效的患者中位总生存期(OS)达32.5个月;
PD-1无效后继续用的患者有效率19%,中位OS 为24.4个月;
PD-1无效后彻底放弃PD-1治疗的患者,中位OS只有11.2个月。
PD-1/PD-L1耐药后更换另一种PD-1/PD-L1可获益
即使是同为PD-1抗体的帕博利珠单抗和纳武利尤单抗在药物结构及药理性质上也存在很大差异,疗效也有所不同。因此,当其中一种药物出现耐药后更换另一种药物也许可以取得不同的治疗结果。
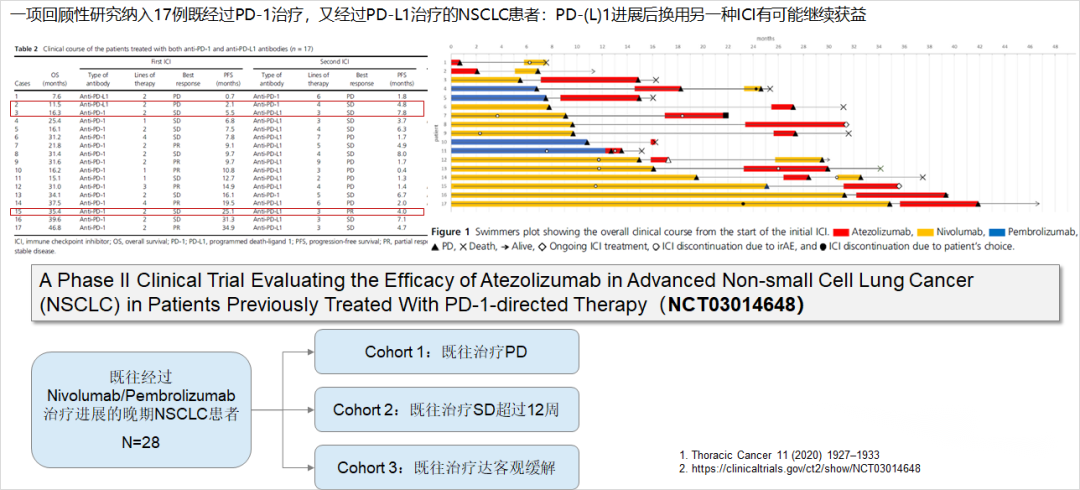
一项纳入 17 例既往经过 PD-1 治疗,之后又用 PD-L1 治疗的非小细胞肺癌患者的回顾性研究显示,部分患者在换用免疫检查点抑制剂(ICI)治疗后也可获益。
PD-1/PD-L1耐药后先穿插其他治疗,后重启PD-1/PD-L1疗效显著
患者在使用免疫药物之前用过放化疗以及联合化疗,能对后续再用PD-1/PD-L1起到一定的治疗增效作用。
一项回顾性研究分析了12例NSCLC患者用O药治疗后再挑战K药的疗效。12例患者中,有8例在O药及K药治疗之间还穿插了其他治疗(化疗为主)。12例患者的客观缓解率(ORR)为8.3%,疾病控制率(DCR)为41.6%,中位无进展生存期(PFS)为3.1个月,K药中位治疗时间为3.5周期。6例患者为PD-L1高表达,DCR为50%。
PD-1/PD-L1耐药后联合局部放疗,ORR达60%
该项回顾性研究纳入207例连续接受O药或K药治疗的晚期非小细胞肺癌患者患者。其中有151例患者接受了O药治疗,56例患者接受K药治疗。研究评估了免疫治疗进展后继续使用的疗效。
共有35例患者(17%)在免疫治疗进展后继续使用原药物治疗,未加入其他新的治疗方式。其中,28例接受O药及7例接受K药。这些患者的临床获益率达到35%(12/35),包括6例PR(部分缓解)和6例SD(疾病稳定)。
有9例患者在免疫治疗首次进展后,针对局部转移病灶进行了放疗,并在放疗后继续使用免疫药物。放疗的时间为进展后的1至2个月。其中有4例患者在放疗后继续了PD1单抗,展现了持久的疗效(8至21个月内都未出现进展)。
所以PD-1耐药后不着急换药,缓慢耐药及寡转移可联合局部治疗继续用免疫药物。
PD-1/PD-L1耐药后联合抗血管生成药物,DCR能达83%
抗血管生成药物可以抑制肿瘤血管生成,改善肿瘤微环境,抑制肿瘤生长和转移。在免疫治疗的基础上,联合抗血管生成靶向药,有望达到更好地控制肿瘤生长的协同增效作用。
在COSMIC-021研究中的队列7,共纳入了30例既往接受过免疫检查点抑制剂治疗的非鳞NSCLC患者,既往治疗线数≤2,接受阿替利珠单抗联合卡博替尼治疗,研究结果显示,ORR为27%,DCR为83%,中位缓解持续时间(DoR)为5.7个月,未出现3级以上的免疫相关不良事件。
MRTX-500研究探索了纳武利尤单抗与Sitravatinib(一种多靶点受体酪氨酸激酶抑制剂)联合用于既往PD-1/PD-L1类免疫治疗进展的非鳞NSCLC。
研究结果显示,在免疫耐药的非鳞 NSCLC 中,联合治疗的ORR为18%,包括2例 CR,DCR为78%,中位DoR 为12.8个月,中位OS 为14.9个月,中位PFS 为5.7个月,进一步验证了免疫联合抗血管治疗模式的疗效获益。
GO30140研究的F队列纳入了119例不可切除的肝细胞癌HCC患者,被随机分为阿替利珠单抗+贝伐珠单抗(n=67)或阿替利珠单抗单药组 (n=52),其中26/52名阿替利珠单抗单药组的患者在疾病进展(PD)后转为接受阿替利珠单抗+贝伐珠单抗治疗。
研究结果显示,在26例患者中,1例患者达到PR(ORR为3.8%),13名患者疾病稳定,DCR达到53.8%,而疾病进展后的剩下26例患者的ORR和DCR分别为0%和30.8%。
对阿替利珠单抗单药治疗耐药的患者,可以通过阿替利珠单抗联合贝伐珠单抗治疗再度获益。
PD-1耐药后,更换CTLA-4抗体或双免疫联合,DCR可达40%以上
一项多中心回顾性研究分析了355名PD-1抗体单药治疗失败的患者,其中230例患者是原发耐药,81例获得性性耐药。分成2组,一组接受单纯的Y药治疗(n=162),另一组患者接受双免疫治疗(n=193)。结果显示:接受Y药单药和双免疫治疗的客观有效率分别是13%和32%,DCR为27%和41%。
PD-1耐药后无论是选择CTLA-4抗体单药还是CTLA-4联合PD-1抗体,患者仍可获益,双免疫联合治疗获益更明显。
一项研究分析了48例恶性黑色素瘤患者在经过PD-1抗体治疗后耐药或者失败的情况下接受Relatlimab(LAG-3抗体)80mg联合PD-1抗体O药240mg治疗后(两周一次,静脉滴注),6位患者肿瘤明显缩小,有效率为12.5%,对于LAG-3表达≥1%的患者,客观缓解率ORR为20%,LAG-3<1%的患者ORR为7.1%,不良反应安全可控。
PD-1耐药后,更换双抗药物,ORR为36%
AK112是一种 PD-1/VEGF双特异性抗体,能同时阻断PD-1和VEGF信号通路,通过改变肿瘤微环境以遏制肿瘤免疫逃逸、释放免疫检查点的免疫抑制以遏制肿瘤血管生成达到抗肿瘤的协同效应。
AK112的I期临床研究,最初剂量递增阶段的临床研究结果令人鼓舞。在对PD-1抗体不敏感或接受过PD-1抗体治疗的11例晚期实体瘤患者中,共有4例患者达到了缓解(ORR为36%), 共7例患者肿瘤缩小且疾病稳定(DCR为64%)。
PD-1/PD-L1耐药后联合化疗,PFS延长
化疗通过细胞毒性直接杀伤肿瘤细胞,并且可以破坏肿瘤细胞的逃逸能力,改变肿瘤微环境,使其更容易被免疫系统识别,因此免疫联合化疗可提高整体抗肿瘤疗效,有效防止肿瘤复发转移。部分临床研究表明,PD-1抑制剂在联合化疗使用后,客观缓解率明显提高且疾病无进展生存期显著延长。
在BTCRC-LUN15-029研究中,将帕博利珠单抗联合化疗用于既往抗PD-1/L1治疗失败的晚期NSCLC,研究结果显示,相比单纯化疗历史对照,帕博利珠单抗联合化疗能够延长既往接受过免疫治疗获益后进展的晚期NSCLC的PFS,中位PFS为5.2个月,中位OS为25.7个月。
当然还有其他多种联合疗法攻克PD-1/PD-L1免疫耐药问题,比如肿瘤浸润淋巴细胞(TIL)治疗、NK免疫细胞回输联合PD-1治疗等等。
相信随着靶向及免疫治疗的发展,越来越多的肿瘤患者生存期会延长。目前国内不限癌种的免疫耐药相关的多项临床试验正在开展,患者均可报名参加。
*声明:本文旨在科普肿瘤医学和新药进展,任何重大医疗决策请前往正规医疗机构就诊。
*版权申明:如需转载请联系小编
