原标题:Cancer Res:靶向乳腺肿瘤代谢弱点 提高治疗效率
本文系生物谷原创编译,欢迎分享,转载须授权!
ShcA接头蛋白负责转导受体酪氨酸激酶下游的癌基因信号。ShcA信号途径如何在乳腺肿瘤中参与癌症发生和发展仍然没有得到深入研究。最近来自加拿大戴维斯夫人医学研究所的研究人员发现ShcA信号途径能够与线粒体代谢核心调控因子PGC-1α共同促进乳腺癌细胞对葡萄糖的利用。相关研究结果发表在国际学术期刊Cancer Research上。
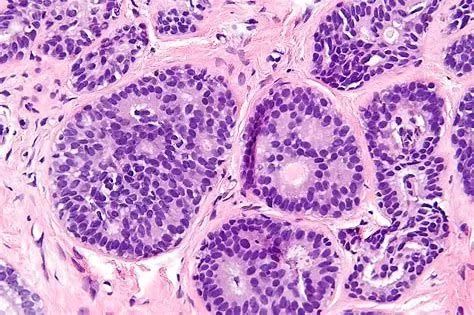
在这项研究中,研究人员发现乳腺肿瘤利用ShcA信号途径增加它们的代谢。ShcA信号能够通过糖酵解和氧化磷酸化增强葡萄糖代谢,导致乳腺癌细胞特别依赖葡萄糖。ShcA信号同时可以诱导线粒体代谢的核心调控因子PGC-1α,增加乳腺癌细胞的代谢速率和代谢的灵活性。借助ShcA信号的乳腺肿瘤极为依赖PGC-1α来支持它们的代谢速率。敲除PGC-1α能够显著延缓小鼠模型体内的乳腺肿瘤发生,表明PGC-1α在肿瘤发生过程中的关键作用。
除此之外,抑制ShcA信号途径可以损伤乳腺癌细胞的代谢速率和代谢灵活性,导致乳腺癌细胞更加依赖线粒体的氧化磷酸化。这种代谢重编程使癌细胞暴露了它们的代谢弱点,导致乳腺肿瘤对线粒体复合物I的抑制剂更为敏感。在Polyoma virus middle T乳腺癌小鼠模型体内在乳腺癌进展的最早期阶段抑制ShcA能够增强乳腺肿瘤对线粒体复合物I抑制剂的敏感性。肿瘤的发生和生长在ShcA敲除小鼠模型体内受到严重损伤。
这些数据表明代谢重编程是与ShcA信号途径有关的一个重要事件,在乳腺癌发生和发展过程中发挥重要作用。这些数据进一步揭示了ShcA和PGC-1α之间在代谢重编程方面的相互作用,提示靶向氧化磷酸化的药物或可有效治疗乳腺肿瘤。
原始出处:
Young Kyuen Im, et al. Interplay between ShcA signaling and PGC-1α triggers targetable metabolic vulnerabilities in breast cancer. Cancer Research, DOI: 10.1158/0008-5472.CAN-17-3696
相关活动推荐
外泌体是细胞主动向胞外分泌的大小均一的囊泡样小体,可以从多种体液中分离。外泌体含有与其来源细胞相类似的细胞因子、生长因子等蛋白质,以及脂质、编码或非编码RNA等生物活性物质。除了用于疾病诊断外,外泌体还具有抗肿瘤免疫,诱导肿瘤免疫逃逸、促进肿瘤血管新生和肿瘤转移等生理功能。随着相关技术快速发展,与液体活检、精准医学和再生医学等领域的不断结合,外泌体的市场预期会大幅增长。
为此,生物谷举办2018外泌体与疾病研讨会,围绕外泌体的生物学功能发现、基础机制,临床应用进展,以及技术开发、产品转化等内容,邀请科研院所知名专家学者、行业领军企业、三甲医院相关科室临床医生等进行探讨,分享最新进展,交流心得经验,促进技术成果的临床转化和应用。
欲参与活动,请点击【阅读原文】


