原标题:【盘点】再生医学中干细胞和新材料的研究和应用
再生医学是目前世界医学研究的前沿。
再生医学是指利用生物学及工程学的理论与方法,促进机体自我修复与再生,或构建新的组织与器官。干细胞具有再生各种组织器官的潜在能力,因此干细胞在再生医学中具有重大的应用价值。
再生医学的优势在于通过改善再生微环境,患者借助自身的再生修复能力引导再生,再生后的组织是人体自身的一部分。随着干细胞和材料科学研究的不断深入,科学家们也尝试着利用材料来模拟干细胞微环境,并不断地取得新的进展。
1.二维细胞培养系统
人们最初尝试着利用二维组织培养系统来模拟干细胞微环境,这是因为它比较简单,易于操作。
比如,2007年4月,庄正陵等人利用低糖DMEM/F12触发多肽自组装为二维凝胶,然后将小鼠神经干细胞接种于多肽二维凝胶表明,结果发现神经干细胞有明显的突起生长,这表明多肽二维凝胶表明不仅有利于神经干细胞(如图1所示)的生长,而且对它们向神经细胞分化有诱导作用。
但是这种二维培养系统并不太适用于研究干细胞行为,这是因为在二维细胞培养系统中,常发生细胞组织架构、机械和生物化学信号以及细胞与细胞之间的信息交流的丢失,无法反映真实组织生理上的复杂性,从而影响细胞功能。
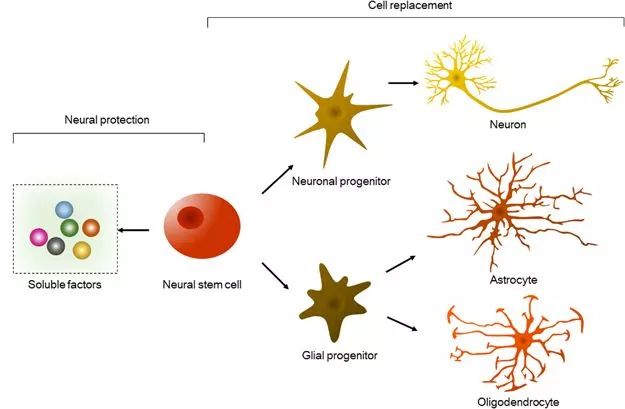
图1.神经干细胞
2.三维支架
三维支架是三维细胞培养时最常用的材料,相当于人工ECM,能够模拟活体组织复杂的三维结构及其主要特征。
三维支架的主要作用是为干细胞提供原始支持,也作为可溶性因子扩散媒介,确保干细胞的粘附、迁移、增殖、分化和长期生存,最终干细胞会形成组织和器官。三维支架具有生物相容性和生物降解性、高度多孔结构、一个相互关联的空隙网以促进养分和代谢产物的交换、适当的力学强度以及适当的表面化学和表面形状以促进细胞的相互作用。
常用的三维支架分为三种:天然ECM支架、天然材料支架和合成材料支架。
目前,人们设计出来的三维支架(3-D scaffold)的数量快速地扩大,包括相对简单的由胶原蛋白制作成的凝胶、聚合物纤维的有序组装或无序组装、水凝胶以及更多。
组织工程的一个关键挑战就是构建三维支架来促进活的干细胞生长,并提供一种合适的环境以便让它们产生活的组织。此外,为了允许干细胞在三维支架中迁移,所设计出来的三维支架通常都是带有孔的,这些孔经常是通过添加盐、糖或二氧化碳气体产生的,但是这些添加物有着很多缺点:它们产生不完整的孔结构而且对盐而言,在孔产生之后还需要采取冗长的工艺去除盐。
2012年2月,Eun Ji Chung等人在真空中采用一种需要高热量的低压发泡(low-pressure foaming)工艺,通过组合使用陶瓷纳米颗粒和弹性聚合物构建出一种新型的三维支架,所形成的这种新型三维支架含有一系列高度相互连接的孔,而且不依赖于盐的使用,此外还能够将它整合到纳米纤维中,从而产生一系列新的机械属性和生物属性。
(1)天然ECM支架
天然ECM支架,也称作脱细胞支架,它的制作过程为从人类尸体后动物组织器官上清除细胞,由此得到的脱细胞支架与天然组织具有极大的结构和机械相似性,是理想的支架系统之一。
2010年9月,英国利兹大学的John Fisher教授及其同事Eileen Ingham教授利用死亡捐赠者或动物的部分身体,将其上所有软组织去除后,仅剩下裸露的结构(即裸露支架),接着来自患者的干细胞就放置在这种裸露支架上,重新长成新的身体部件。这种方法的优点是,因为支架上已被剥离了所有能触发排异反应的材料,而软组织则是从患者自身干细胞培育出来的,所以患者不会将移植组织作为外来物而加以排斥。这意味着,患者将能避免使用可缩短预期寿命和增加癌症风险的强力免疫抑制药物。该项技术已成功地为那些遭受创伤和疾病的患者创建出一段新气管,并有望用于创制更广范围的人体器官。
2010年10月,美国维克森林大学医学院主管兼教授Shay Soker团队使用人体干细胞制造出微型人体肝脏,在一个“支架”上形成新的肝脏组织,而这个“支架”由一个动物肝脏制造而成,如图2所示。具体而言,他们首先将动物肝脏中的细胞除去,仅仅留下支持细胞生长的胶原蛋白框架以及一个细小的血管网络。接着将新的干细胞,也就是不成熟的人类肝脏细胞和内皮细胞(主要用于形成血管的内壁)逐渐填入“支架”中。随后,再将整个支架移入一个生物反应器中,并使用营养物质和氧气的混合物来培养这些细胞。一周后的观察发现,细胞的生长状况非常好,甚至表现出了很多真正人体肝脏的功能。
图2. 利用雪貂肝脏制备含有血管的脱细胞支架并进行超微结构分析
脱细胞支架保留了组织或细胞特异性的ECM蛋白组分和微结构,因而得到广泛应用,但是它的缺点在于天然组织的质量难以控制,天然组织结构本身是非常复杂的,实际制备过程对技术要求比较高。
(2)天然材料支架
用于构建天然材料支架的天然材料来源于细胞或组织,包括动物源性I型胶原蛋白及其基底膜提取物,从海藻中提取的藻酸盐,蟹壳虾壳中提取的壳聚糖等。天然材料支架分为单源性天然材料支架和混合天然材料支架。单源性天然材料支架指的是用来源于细胞或组织的天然材料(如胶原蛋白、基质胶和藻酸盐等)制成的。混合天然材料支架指的是的除了天然材料之外,还有合成材料(比如合成的基底膜)的存在。
2012年3月,Hong Fang Lu等人将一种带正电荷的被称作几丁质的生物聚合物(从蟹壳中提取出来的)和一种带负电荷的被称作海藻酸钠(sodium alginate)的聚合物的液滴加到无菌的基质上,从而形成几丁质-海藻酸钠复合物。基于分子间静电引力,这种复合物能够延伸成连续性的纤维。随后,他们将这种纤维卷到一种支撑物(holder)上,从而获得一种新型的三维支架。移植到这种三维支架上的干细胞能够大量生长,而且当经过多次传代培养后,被包裹的干细胞仍然保持多能性,而且并不产生任何基因突变。再者,依赖于所获得的培养基,干细胞能够自我更新或者分化。
2013年2月,Kate A. Meade等人开发出一种类似于网状的支架,其由糖衣分子包被,可以增强干细胞的培养环境。这种支架是由一种名为“静电纺丝”的结构所形成,其可以产生类似于机体结构的网状纤维。这些网状纤维可以通过长链、线性的糖分子来修饰,此前的研究结果显示,糖分子在调节杆细胞行为上扮演着重要的角色。通过将糖分子结合至纤维网络中,人们希望使用生化和结构信号来指导干细胞的行为,类似于在集体中那种天然的行为模式,这将成为使用干细胞技术开发新型疗法研究的圣杯。
2014年7月17日,中国科学院遗传与发育生物学研究所戴建武团队用自身骨髓干细胞复合胶原生物支架修复子宫内膜之后,一名产妇在南京鼓楼医院成功产下一名健康男婴,这也是世界上第一例在干细胞修复子宫内膜技术下诞生的婴儿。同年10月30日,第二例婴儿又成功分娩。这标志着该技术具有充分的临床可行性,是世界再生医学领域的重大突破。
2015年1月17日,中国科学院遗传与发育生物学研究所在天津宣布,世界首例使用神经再生胶原支架结合间充质干细胞治疗脊髓损伤临床研究取得成功。这种神经再生胶原支架是戴建武团队经过十余年努力研制出的基于胶原蛋白的神经再生支架,如图3所示。
在此次临床研究之前,该团队已首创大鼠及比格犬长距离脊髓全段缺损的损伤模型,研究神经再生胶原支架及其功能化型式(如结合生长因子或者干细胞)引导神经再生以及脊髓损伤功能的恢复。长期观察试验中发现能够有效促进动物运动功能恢复,包括站立及行走。
同年,戴建武团队设计了可注射智能型胶原支架材料,以水凝胶形式存在,接着让脐带间充质干细胞附着在这种可降解的胶原支架材料上并注入患者卵巢内,形成一个供干细胞生长发育的“温床”,就这样利用支架帮助干细胞定植、分化,激活原始卵泡,修复早衰的卵巢,从而使卵巢早衰的女性能够重新获得生育的能力。此外,胶原支架在完成“任务”之后,通常持续数月左右就会自然降解,对人体无伤害。
图3. 神经再生胶原支架.(A为实体图, B为电镜下照片; 图片来自参考文献15)
鉴于天然材料来源于细胞或组织,能够促进细胞形态发生,提升细胞功能,降低脱细胞天然支架的复杂性,但是它本身复杂的生化反应、质量不一致、不明确来源等数量限制了它的应用。
(3)合成材料支架
合成材料支架具有良好的可控性和降解性,精确的组成组分和物理特性,可操作性高,灵活大,没有免疫方面的问题。聚乳酸羟基乙酸(PLGA)、聚乙醇酸(PGA)、聚L-乳酸(PLLA)和聚己内酯(PCL)、聚醚和聚碳酸酯等合成可降解高分子材料已被应用于合成材料支架(比如PLGA支架、PCL支架和PLLA支架等)的构建和组织工程学的相关研究。
除此之外,合成材料还包括合成可降解无机材料,常用的主要有磷酸钙水泥(calcium phosphate cement,CPC),羟基磷灰石(hydroxyapatite,HA),磷酸三钙( tricalcium phosphate, TCP),生物活性陶瓷如生物活性玻璃陶瓷( biological activity ceramic glass,BCG)和细胞外基质陶瓷类材料等。
2011年6月,Huixia He等人发现相比于羟基磷灰石/磷酸三钙支架,粘附到一种新的支架---纳米羟基磷灰石/胶原/聚乳酸支架---上的狗牙周膜干细胞的数量更多,增殖活力更强,可以作为一种牙槽骨再生的高效能支架。
图4.在不存在成骨添加剂(osteogenic supplement, OS)的情形下,hBMSC在组织支架上培养1天或50天时的荧光显微图(40×)。
2011年12月,Girish Kumar等人比较了5种流行的由生物相容性聚合物聚己酸内酯(polycaprolactone, PCL)或聚内消旋乳酸(Poly-D/L-lactic acid, PDLLA)组成的组织支架对人原代骨髓基质细胞(primary human bone marrow stromal cells, hBMSC)---它是一种成体干细胞,能够从骨髓中分离出来,而且能够依据不同条件分化为骨细胞、脂肪细胞和软骨细胞---的影响,如图4所示。他们发现改变支架的结构能够改变hBMSC的形态,从而控制hBMSC的分化途径,产生所需的分化细胞,而在这一过程中除了所需的细胞生长培养基外,还不用添加生物化学添加剂,从而可以避免加入生物化学添加剂可能带来的副作用。
2013年1月,Rong Zhang等人鉴定出一组基于2-(二乙胺基)丙烯酸乙酯的热反应性合成水凝胶,发现它们支持在2至6个月内促进人类胚胎干细胞生长和维持它们的多能性。
合成材料支架的缺陷在于器官特异性结构和细胞类型特异性的相对缺乏。因此,合成生物材料支架需要经过修饰后携带整合素结合肽、生物因子结合位点、促进细胞-ECM相互交联的ECM降解蛋白酶结构域等。
(4)石墨烯三维支架
石墨烯为单层或少层碳原子组成的低维碳纳米材料,具有优异的理化性质,自2004年被发现以来,已迅速成为材料科学与凝聚态物理等领域的研究对象。同时,石墨烯能够表现出良好的生物相容性,已被用于细胞成像、药物输运、干细胞工程及肿瘤治疗等领域。
2013年,中科院苏州纳米所程国胜团队与中科院遗传与发育研究所戴建武团队合作,成功开发出新型石墨烯三维神经支架材料,如图5所示,结果表明这种三维石墨烯支架不仅能促进神经干细胞的增殖,还能够在一定程度上诱导神经干细胞定向分化为功能神经元。他们进一步利用石墨烯碳材料良好的导电特性,对神经干细胞进行原位电刺激和诱导分化,成功获得了可逆特性的钙离子振荡响应。
图5.石墨烯三维神经支架的扫描电镜显微图.
(5)三维打印支架
三维打印常常被认为具有通过再生性植入物颠覆医学世界的潜力,甚至有可能导致人造器官和组织的出现。在全世界有多家研究机构都在进行着三维打印细胞结构的研究竞赛。近年来,科学家在利用三维打印制备三维支架上不断地取得进展。
2016年,荷兰马斯特里赫特大学Lorenzo Moroni实验室的研究人员展示了三维打印技术是如何能够被用来设计和制造带有嵌入结构和物理-化学梯度的支架,如图6所示。
据悉,正是这些梯度影响着成体间充质干细胞朝着骨细胞方向的分化。他们展示了孔隙大小和形状的梯度能够影响成体间充质干细胞朝着骨细胞方向的分化。更重要的是,这是一个相当灵活的过程。三维打印支架的孔隙尺寸可以增加或减少,从而让间充质干细胞分化成骨或软骨。同样地,当孔隙形状从偏正方形变化到更偏菱形形状时,间充质干细胞的分化方向也会从软骨逐渐转向骨。
图6.三维打印支架。
更好地控制干细胞与三维支架材料之间的相互作用是维持组织结构所必要的。它是控制干细胞在三维支架中休眠、增殖和分化,同时将细胞保持在原位的关键。在这个过程中,三维打印可以发挥巨大的作用,但新的技术和硬件的开发仍是必需的。
小结
考虑到干细胞微环境的复杂性,在体外复制这样的干细胞微环境不仅仅需要我们对生物学有非常深入和透彻的理解,同时还得具备按照我们的意愿,打造出这样一套能够行使恰当生物化学和生理学功能的立体生态结构的能力,而材料科学专业知识和技能就是其中不可或缺的一个必备条件。
随着干细胞、材料工程学、生物技术、物理化学、电子、三维打印技术、计算机辅助设计等技术研究的不断深入,相信在不远的将来可以实现再生医学的终极目标,即修复或再生各种组织和器官,解决因疾病、衰老、创伤或遗传因素造成的组织器官缺损和功能障碍。
为此,生物谷将于2018年11月9日至2018年11月10日在北京举办第十届干细胞国际研讨会,本届干细胞国际研讨会在秉承此前干细胞临床与转化的会议经验基础上,我们围绕干细胞重编程与再生医学、干细胞临床研究即干细胞商业化等多个领域,邀请国内外知名专家学者、业界翘楚、临床医生一道进行深入讨论,促进合作交流。同时本次研讨会特别设立“青年千人”论坛,为海内外优秀青年学者搭建学术交流平台。
重要会议推荐: 2018(第十届)干细胞国际研讨会
会议亮点
1.探讨干细胞基础研究的热点与难点
围绕干细胞重编程、干细胞干性维持与定向分化,干细胞与组织器官修复、类器官等进行深入交流
2.推动干细胞治疗的临床转化
围绕干细胞临床转化过程中遇到的问题, 邀请专家、临床医生等解答
3.促进干细胞治疗的完善与发展
讨论干细胞治疗规范和标准, 干细胞的存储、制备的自动化
会议时间:2018年11月9日-10日
会议地点:北京元辰鑫国际酒店
联系邮箱:fan.peng@bioon.com
联系方式:17321098232
参考文献:
1.Natalie de Souza. (2013) In vitro niches. Nature Methods, 10:37.
2.邱云等. 干细胞微环境的体外模拟. 中国组织工程研究, 2011, 15(6):1123-1126.
3.Tanya M.Farooque et al. Measuring stem cell dimensionality in tissue scaffolds. Biomaterials, March 2014, 35(9):2558-2567.
4.Basak E Uygun et al. Organ reengineering through development of a transplantable recellularized liver graft using decellularized liver matrix. Nature Medicine,2010,16814-820.
5.Huixia He et al. Biocompatibility and Osteogenic Capacity of Periodontal Ligament Stem Cells on nHAC/PLA and HA/TCP Scaffolds. Journal of Biomaterials Science Polymer Edition, 2011, 22(1-3):179-94.
6.庄正陵等人. 多肽二维凝胶支架材料与鼠神经干细胞的细胞相容性. 华中科技大学学报(医学版), 2007年4月,36(2):217-219.
7.Eun Ji Chung et al. Low-pressure foaming: a novel method for the fabrication of porous scaffolds for tissue engineering. Tissue Engineering Part C: Methods, Feb. 2012, 18(2).
8.Hong Fang Lu et al. A 3D microfibrous scaffold for long-term human pluripotent stem cell self-renewal under chemically defined conditions. Biomaterials, March 2012, 33(8):2419-2430.
9.Rong Zhang et al. A thermoresponsive and chemically defined hydrogel for long-term culture of human embryonic stem cells. Nature Communications, 2013, 4(1):1335.
10.Kate A. Meade et al. Immobilization of Heparan Sulfate on Electrospun Meshes to Support Embryonic Stem Cell Culture and Differentiation. Journal of Biological Chemistry, 22 February 2013, 288:5530-5538.
11.李彤等人. 三维细胞培养中支架的研究现状. 北京生物医学工程, 2017, 36(4) :433-437.
12.Ning Li et al. Three-dimensional graphene foam as a biocompatible and conductive scaffold for neural stem cells. Scientific Reports, 2013, 3, 1604.
13. Shay Soker et al. The use of whole organ decellularization for the generation of a vascularized liver organoid. Hepatology, 2011, 53(2):604-617.
14. John Fisher et al. Investigation of the Regenerative Capacity of an Acellular Porcine Medial Meniscus for Tissue Engineering Applications. Tissue Engineering Part A, January 2011, 17(1-2):231-242.
15. Jianwu Dai et al. One-year clinical study of NeuroRegen scaffold implantation following scar resection in complete chronic spinal cord injury patients. Science China(Life Sciences), July 2016, 59:647-655.
16.Girish Kumar et al. The determination of stem cell fate by 3D scaffold structures through the control of cell shape. Biomaterials, December 201,32(35):9188-9196.
点击阅读原文,围观更多精彩!







