传统观点认为,体育锻炼对心脏健康有益,有助于降低心血管疾病发病率和死亡率。然而,近年研究表明过度运动可能对心脏产生不利影响。
《NEJM循证》发表的一篇综述提示剧烈耐力运动增加心肌细胞损伤标志物,指出终身耐力运动可能增加心肌瘢痕、冠状动脉粥样硬化、房颤和主动脉扩张等疾病风险,并介绍这些疾病的治疗方法。我们在此简介该综述。
前言
Jeremy Morris教授作为伦敦公务员运动获益研究的负责人,将体育锻炼视为“公共健康的最佳投资”。多项流行病学研究表明,热衷于体育锻炼的人群相较于不爱运动者,其心血管疾病(CVD)发病率降低40%~50%,因此,这一论断确有依据。体育锻炼对公共健康带来重大益处的部分原因在于,发达国家的久坐生活方式日益普及。流行病学研究指出,特别不爱运动和稍有运动的个体是降低心血管疾病风险的重要对象。随着运动量增加,风险不断降低,但降低幅度逐渐减小;有研究甚至显示,当活动量达到最高水平时,风险会趋于稳定或略有增加。鉴于体育锻炼量较大的人群相对较少,关于过量运动可能带来风险的报告有限。最新的《美国人体育锻炼指南》着重强调了适度增加运动量的益处。该指南建议美国人“多活动、少久坐”,每周进行150~300分钟的中度(如快走)或75~150分钟的剧烈(如慢跑)有氧运动,每周进行两次阻力训练,老年人进行一定量的平衡训练。
对运动过量的担忧自古就有。这些担忧在维多利亚时代的英国再次浮现,当时社会精英开设的学校和大学开始开展跑步、骑自行车和划船等运动项目的竞赛,而这些运动以前都是工人阶级开展的与工作相关的比赛。成年人剧烈运动可能诱发急性心肌梗死(AMI)和心脏性猝死(SCD)。与运动相关的ST段抬高型急性心肌梗死通常是由于动脉粥样硬化斑块破裂导致急性冠状动脉血栓形成,而SCD则与急性冠状动脉斑块破裂和/或慢性冠状动脉疾病(CAD)有关。年轻患者的SCD很少由动脉粥样硬化性CAD引起,最常见的原因是遗传、先天性和后天性心脏病。最近的研究还表明,长时间剧烈有氧运动会导致急性心肌细胞损伤、心肌纤维化、冠状动脉钙化(CAC)、心房颤动(AF)和主动脉扩张。本综述总结了运动与这些疾病相关的证据,并概述了这些疾病的治疗策略。
一次耐力运动后心肌肌钙蛋白升高
完成42公里跑步比赛(马拉松)后,肌酸激酶(CK)水平会升高,这一观察结果表明长时间运动会对心肌细胞造成损伤。一项针对参加1979年波士顿马拉松比赛的15名医生的研究发现,使用总CK诊断急性心肌梗死时,CK水平从赛前的161 U/L升至赛后第二天的3424 U/L(正常范围<100 U/L)。随后的研究使用心脏特异性更高的CK-MB,结果显示,CK-MB从赛前的6.9±6.4 U/L升至赛后的105.3±99.3 U/L(正常范围<5 U/L)。
马拉松运动员腓肠肌活检标本中的CK-MB浓度是久坐不动对照组活检标本的两倍多(8.9±1.3% vs. 3.3±0.7%),这表明运动训练会增加骨骼肌CK-MB浓度。卫星细胞能够修复受伤的骨骼肌并产生CK-MB,在跑步者的活检标本中也存在卫星细胞。这些发现提出了一种理论,即训练会损伤骨骼肌,需要卫星细胞进行修复,从而在随后的运动中释放出CK-MB。心肌细胞损伤的可能性在很大程度上被否定了,直到1996年心肌肌钙蛋白(cTn)的检测方法问世,并取代CK-MB成为心肌损伤的生物标志物。
肌钙蛋白(Tn)是Tn-肌球蛋白肌肉收缩复合体的一部分。在三种Tn亚基(C、T和I)中,只有T和I具有骨骼肌和心肌特异性亚基,可用于诊断心肌损伤。一份报告指出,在74名骨骼肌病患者中,仅有4人的静息cTnI值超过正常范围上限,而67名患者的cTnT值超过正常范围上限。
有200多篇文献对运动后的cTn进行了测量,并反复证明cTnT和cTnI均可升高。这些研究涉及各种耐力运动后的患者。在马拉松等长时间耐力运动后,超过50%参与者的cTnT和cTnI水平超过了急性心肌梗死的诊断水平。一项马拉松研究表明,所有选手在赛后的cTnI都有一定程度的升高(图1)。由于年龄、性别、训练状况、健康状况和环境条件等多种因素的影响,cTn升高在个体间存在很大差异,但运动强度和持续时间是最重要的决定因素。
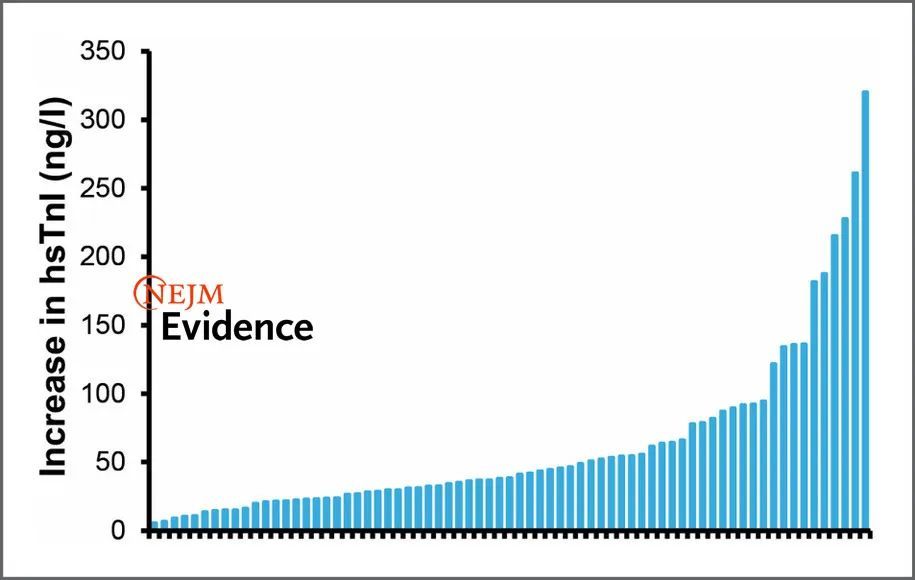
图1. hsTnI 水平的变化。
数据来自2011年波士顿马拉松比赛的71名参赛选手从赛前到赛后的数据。hsTnI表示高敏心肌肌钙蛋白I。
运动引起cTn升高的机制尚未完全明确。cTnI升高很可能由心脏引起,因为目前尚未有任何研究表明训练会像增加CK-MB水平那样增加骨骼中TnI的含量。Tn存在于与肌球蛋白结合的心肌细胞中,可以在细胞质中自由循环。运动会导致含有肌动蛋白的囊泡释放,这可能是为了细胞间信号传导。拉伸或可逆性损伤导致心肌细胞肌浆通透性发生变化,未结合的cTn或cTn片段可能会释放至血液中。也有人推测运动后出现不可逆的心肌细胞凋亡和/或坏死,但考虑到耐力运动后cTn常常升高,这种推测不太可能成立。
与运动相关的cTn增高不会造成严重不良后果,但静息cTn水平是一种心脏风险标志物。一项回顾性分析纳入21项前瞻性研究,对普通人群中的64,855名无症状者进行了cTn检测。其中5%参与者的cTn水平高于第99百分位数,并且与总死亡率和心血管疾病死亡率增加3倍相关。仅检测到cTn就会导致心血管疾病死亡率增加30%,而且随着cTn水平升高,风险也会逐渐增加。
为了避免急性心肌梗死的过度诊断,临床医生应该知道耐力运动会导致cTn水平升高,但这些数据的长期影响尚不清楚。在一项研究中,725名参与者(年龄在54岁~69岁之间)中有63人在步行30~55公里后,cTn水平立即超过第99百分位数。运动后cTn水平小于或大于第99百分位数的参与者中,分别有7%和27%的人在随访期间发生了主要心血管疾病事件(图2)。在对年龄、性别、心血管疾病风险因素、既往疾病和基线cTnI进行调整后,风险仍然较高(HR,2.48;95% CI,1.29~4.78)。这些数据表明,运动后cTn水平升高可能会确定哪些人有发生心血管疾病的风险,但这是一个老年人群,而且不是耐力运动员,因此这些数据还需要进一步确认。
图2. Kaplan–Meier结局。
图示为725名步行30~55公里的参与者在事件发生前后心肌肌钙蛋白I值高于(红色)或等于或低于(蓝色)第99百分位数。
耐力运动对右心室的急性影响
耐力运动训练可降低心率(HR),并导致四个心腔均扩大。这种运动诱导的心脏重塑有助于增加每搏输出量(SV),以维持静息时的心输出量,并提高运动高峰时的心输出量,因为运动训练不会增加最大心率。
耐力运动也会产生急性心脏变化。超声心动图研究显示,在长时间运动后,左心室收缩和舒张功能的急性下降幅度较小,但右心室功能的下降幅度却很大。对完成夏威夷铁人三项赛的运动员进行的早期检查发现,赛后左心室、左心房和右心房的容量立即缩小,而右心室的容量扩大,这表明右心室的收缩能力下降。比赛结束28小时后,右心室容量恢复到赛前值。随后的研究证实,在长时间运动后,右心室功能的下降幅度大于左心室功能的下降幅度,并且右心室功能的下降可能与cTnT和cTnI的变化成反比。心室功能的下降随着运动持续时间和运动员最大摄氧量的增加而增加,这意味着运动能力最强的运动员最容易发生右心室功能下降。
耐力运动对右心室的影响可能是由于血管对运动的反应不同造成的。由于肺循环的血管扩张能力有限,肺血管阻力在运动时仅下降30%~50%,而由于运动肌肉的血管扩张,全身血管阻力下降超过75%。据估计,右心室壁应力增加约170%,而左心室壁应力仅增加约23%。此外,运动训练可增加全身血管舒张能力,但对肺血管阻力影响甚微。运动训练能增加最大SV值和最大摄氧量,这意味着优秀运动员可将更大的SV泵至基本保持不变的肺循环中。
运动对右心室的急性和慢性影响对心律失常性右心室心肌病患者具有重要的临床意义。桥粒蛋白的遗传性缺陷会导致这种心肌病,但携带类似基因突变的个体在临床表现上存在很大差异。心律失常性右心室心肌病的小鼠研究和临床研究均表明,大量运动与疾病早期发作和进展迅速相关。目前的指南建议患有这种心肌病或有这种遗传风险的患者不要进行剧烈运动。
运动员的心肌纤维化
钆增强心脏磁共振成像(cMRI)可识别心肌瘢痕和纤维化。正常心肌的肌动蛋白呈线性,无法保留钆,而纤维化组织则会保留钆,出现晚期钆增强(LGE)。一项对运动员cMRI检查的荟萃分析纳入14项研究和1,342名参与者。结果显示,16.6%的运动员和2.3%的对照组参与者出现了LGE(P<0.001)。另外,7%的运动员和0.3%的对照组参与者的LGE位于RV与室间隔移行处(P=0.003,图3)。即使排除在RV与室间隔移行处出现LGE的运动员,LGE在运动员中仍然更为普遍。在女性运动员中,LGE的发生率没有增加,但由于研究只包括119名女性运动员和82名对照组参与者,结论或许受到样本量不足的影响。在年轻运动员中也观察到了无法解释的LGE。另外一项针对2019冠状病毒病康复期大学生运动员的研究中,60名未受感染的对照组运动员也接受了cMRI检查,其中有10人(24%)在RV与室间隔移行处显示出LGE。荟萃分析显示,年龄小于40岁的运动员(25.7%)的LGE发生率高于年龄>40岁的运动员(14.6%)。这些发现对年轻运动员的临床意义尚不清楚。
图3. 一名正常人和五名耐力运动员的cMRI。
心脏磁共振成像(cMRI)显示室间隔内晚期钆增强,通常是在右心室室间隔移行处。
耐力运动员RV与室间隔移行处LGE的流行率与运动时RV容积和室壁应力急剧增加导致该部位纤维化的观点一致。然而,这些发现的临床意义尚不确定,需要进行更严格的随访研究。临床医生应注意,无症状的运动员可能在RV与室间隔移行处出现LGE。有报道称,有LGE的跑步者预后较差,但这些参与者的LGE并不局限于移行处,40%跑步者的LGE模式是典型的冠状动脉疾病(CAD)引发的纤维化。
耐力运动员中的CAC
Clarence DeMar曾七次夺得波士顿马拉松赛冠军,并在69岁之前一直参加竞技比赛。他在70岁时死于结肠癌。波士顿著名心脏病专家Paul Dudley White报告了DeMar的尸检结果,并指出DeMar的冠状动脉是正常大小的2~3倍,左主干管壁有相当程度的动脉粥样硬化,但管腔通畅性仍然良好。
随后的报告肯定了运动训练对冠状动脉直径和血管活性的益处,但最近的研究报告了终身运动训练可能导致冠状动脉钙化(CAC)和动脉粥样硬化风险增加。一项研究采用CAC和计算机断层扫描冠状动脉造影测量冠状动脉粥样硬化程度,进而分析耐力运动训练与冠状动脉粥样硬化的相关性,结果发现,中年耐力运动员的CAC和冠状动脉粥样硬化程度高于对照组参与者,而运动量最大运动员的CAC和冠状动脉粥样硬化程度最高。运动员的冠状动脉斑块多为钙化,而非钙化或混合型斑块较少,这意味着动脉粥样硬化斑块更为稳定(图4)。女性的相关研究数量较少,但现有数据提示动脉粥样硬化没有增加。
图4. 耐力运动员与对照组冠状动脉粥样硬化斑块特征的比较
运动员动脉斑块增多的预后尚不明确。钙化斑块被认为比较稳定,但一项小型研究表明,大量运动会刺激软斑块形成。全美长跑比赛是一项为期140天的徒步比赛,参赛者每天跑步25.7英里,每周休息一天。10名参赛者中有8人完成了比赛,并在赛前和赛后接受了计算机断层扫描冠状动脉造影。基线没有CAD的参赛者的冠状动脉粥样硬化并未加重,但所有基线有CAD的参赛者在赛后的冠状动脉粥样硬化都有所加重,主要是因为非钙化斑块的增加。
至少有一项研究考察了无症状、活跃男性参赛者中CAC增加的预后。在最活跃的参赛者中,CAC评分较高,但这与总死亡率或CAD死亡率在统计学上无显著相关性。然而,在最活跃组中,CAC评分大于或小于100 Agatston单位的心血管疾病死亡率分别是最活跃组的9倍(1.8和0.2/1000人-年)。虽然这在统计学上并不显著,可能是因为事件发生率较低,但表明即使在高度活跃的人群中,CAC评分增加也可能有害。
导致耐力运动员动脉粥样硬化和CAC增加的因素尚不确定。运动时心率和血压的急剧升高可能会增加动脉剪切应力。长时间运动也会使炎症标志物急性但短暂地升高。与跑步者相比,骑自行车者的斑块似乎较少,这可能与脚部撞击导致的动脉血流动力学或钙代谢变化相关。运动也会使甲状旁腺激素水平急剧升高,这可能会加速动脉粥样硬化的钙化,但并不能解释动脉粥样硬化加重。耐力运动员的心脏体积增大,可能会增加冠状动脉的偏移和弯曲,从而产生更多湍流,加速胆固醇沉积。
对无症状CAC和冠状动脉粥样硬化运动员的管理以共识建议为基础,但应包括排除运动诱发的缺血和积极的CAD危险因素管理。是否允许这些人继续参加运动取决于与运动相关的CAD事件风险以及与运动员共同做出的决策。
心房颤动
活动量与心房颤动之间的关系复杂,值得深入探讨。在男性中似乎呈U型,这意味着随着低水平活动量增加至中等活动量,心房颤动风险逐渐减少,但随着活动量增加和/或高强度运动,风险可能保持不变,甚至会增加。与此相比,女性在各种活动量下的房颤风险似乎都有所降低。一项对运动员房颤风险的荟萃分析发现,他们的房颤风险增加了5倍。另一项涵盖了19项研究的荟萃分析表明,相较于不太活跃的人群,每周进行5至20个代谢当量小时的体育锻炼可以降低房颤风险,但每周超过20个代谢当量小时的人群并没有观察到房颤风险降低。
在瑞典Vasaloppet越野滑雪赛的研究中发现,随着运动量增加,房颤发生率也会增加。研究人员利用国家医疗数据库对滑雪者和匹配对照组参与者的临床结局进行了比较。结果显示,女性滑雪者的房颤发生率低于非滑雪者,而经过房颤风险因素调整后,男性滑雪者的房颤发生率较高。值得注意的是,完成比赛次数最多且成绩最好的男性运动员的房颤风险也更高(图5)。尽管男性和女性滑雪运动员的卒中发生率较低,但房颤患者卒中的频率却高于非房颤者,这表明运动员的房颤并非无害。
图5. 参加Vasaloppet国际滑雪节乡村滑雪赛的男女选手心房颤动的风险。
耐力运动员房颤风险升高的机制尚不清楚。运动训练导致副交感神经张力升高,急性运动引起交感神经张力升高,这些均可能增加房颤风险,而运动引起的急性炎症也可能其机制之一。由于每搏输出量是运动能力的指标之一,而在最活跃和最成功的运动员中观察到房颤发生率增加,因此耐力运动训练导致的心房扩大可能是房颤风险升高的因素之一。对于运动员房颤的管理应遵循普通人群房颤的治疗指南。
主动脉扩张
参与体育运动对年轻运动员的主动脉直径影响似乎较为有限。一项荟萃分析对运动员和对照组参与者主动脉直径进行了评估,结果发现运动员的主动脉在Valsalva窦和主动脉瓣环处的直径仅分别增大了3.2 mm和1.6 mm(P=0.02和P=0.04)。虽然这些变化轻微,但它们可能有长期意义。
有人通过计算机断层扫描成像比较了前职业美式橄榄运动员和对照组参与者的主动脉中段直径(平均年龄分别为57.1岁和53.6岁),发现前者的主动脉直径更大(38±5 mm vs. 34±4 mm;P<0.001)。球员中主动脉直径大于40 mm的比例更高,即第99百分位数(29.6% vs. 8.6%;P<0.0001)。然而,这种扩张可能与运动无关,而与其他因素有关,包括在活跃的美式橄榄球运动员中普遍存在的高血压。一项针对大部分澳大利亚橄榄球退役运动员(平均年龄为45±13岁)的超声心动图研究显示,41%运动员的主动脉直径大于40 mm,58%运动员的主动脉窦管交界处前部膨出,这是主动脉异常扩张的一个指标。主动脉扩张与球员职业生涯的长短有关,而在精英球员中,主动脉扩张更为常见。
这些研究针对参与运动项目的个体进行了检查,这些个体的训练和比赛主要涉及阻力运动,而阻力运动会导致收缩压急剧升高。一项针对442名年龄为61±6岁的赛艇运动员和跑步运动员的超声心动图研究发现,31%男性和6%女性主动脉直径大于40 mm。主动脉直径增大在精英运动员中更为常见,而且随着运动训练年限的增加而增大。
这些观察结果的临床意义尚不清楚。优异的运动成绩与主动脉增大的幅度直接相关,这再次提出了一种可能性,即运动训练量或为取得优异成绩而增加的每搏输出量是导致主动脉扩张的原因之一。对于运动员主动脉扩张的处理应遵循普通人群的指南。
结论
增加运动量和锻炼与降低心血管疾病发病率和死亡率相关。然而,越来越多的证据表明,耐力运动可能会导致急性心肌损伤指标升高,并在急性期降低右心室功能。长期的运动训练也与轻度心肌纤维化、冠状动脉粥样硬化和冠状动脉钙化增加、房颤发生率增加以及主动脉扩张相关。这些影响的临床意义尚不确定,但它们提供了进一步研究大量运动训练对健康的长期影响的机会。临床医生应了解这些可能由运动引起的训练效应,以便为中年运动员提供适当的管理。
参考文献
1. Thompson PD, Eijsvogels TMH, Kim JH. Can the heart get an overuse sports injury? NEJM Evid 2023;2:EVIDra2200175.